
水凝胶包裹的脐带间充质干细胞来源的外泌体通过增强血管生成来加速骨修复

杂志:ACS Applied Materials & Interfaces
IF:9.229
发表时间:2021.04
研究背景
由创伤、肿瘤和畸形引起的大骨缺损的修复一直是骨科医生面临的主要挑战之一。目前,自体骨移植是治疗骨缺损的最佳方法;然而,由于资源有限和并发症复杂,自体骨移植的应用受到严重限制。
骨组织工程(BTE)是一种有效的替代方案,它使用支架和天然或合成分子的结合来促进骨再生,但是,组织工程支架中缺乏血管形成是导致再生效率低和这一治疗方案失败的主要原因。血管生成是骨再生过程中必不可少的一部分。考虑到血管在各种细胞营养中的重要作用,开发促进血管生成的新技术被认为是BTE成功的关键。
随着人们对间充质干细胞(MSCs)的深入了解,越来越多的研究集中在外泌体释放对间充质干细胞的治疗益处上,外泌体是一种直径为30-200nm的膜结合囊泡;外泌体包含各种功能蛋白、mRNA、microRNA和脂质,被认为是组织修复策略中高效无细胞治疗应用的一个非常有吸引力选择。MSC来源的外泌体在血管形成、发育和进展中有积极作用。
目前,用于治疗的外泌体仍处于起步阶段。主要的应用方式是直接注入和载体加载。直接注射主要针对全身性疾病,如骨质疏松、血液系统恶性肿瘤、心肌缺血再灌注损伤。组织损伤的修复,特别是骨的修复和再生,是一个长期的、复杂的多阶段的过程。生物医学水凝胶,如透明质酸、壳聚糖和聚乙二醇,在结构上与天然细胞外基质(ECM)相似,具有良好的亲水性、生物相容性、生物降解性和包封能力,它们被认为是很有前途的生物材料,可以在BTE中传递药物/细胞因子/细胞。
然而,与其他可生物降解的水凝胶类似,这些材料无法保持其形状。因此,一种合理的方法是结合合成支架,形成一种具有高细胞相容性和良好力学性能的混合复合材料。
本研究通过3D打印技术制备了定制的纳米羟基磷灰石/聚-ε-己内酯(nHP)支架。然后,用uMSCEXOs封装的可注射的透明质酸(HA)水凝胶(Gel)完全填充了nHP支架的孔隙结构。最终,我们在大鼠临界大小的颅骨缺损模型中观察并评估了该复合缓释系统的生物材料特性和促血管生成功能。
研究流程图
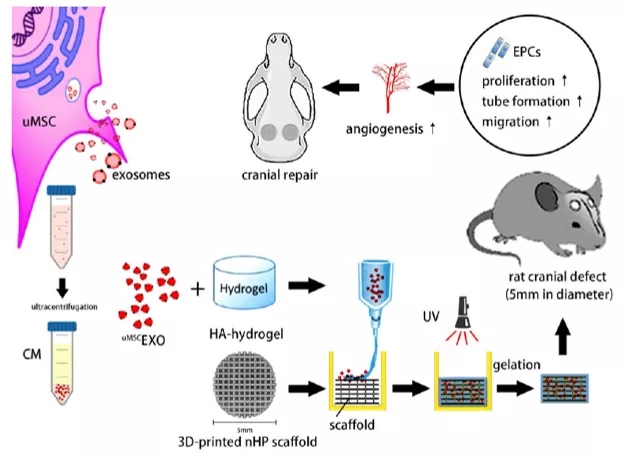
研究核心内容

研究结果分析
一、水凝胶/nHP支架复合材料的制备
1.外泌体的分离与鉴定
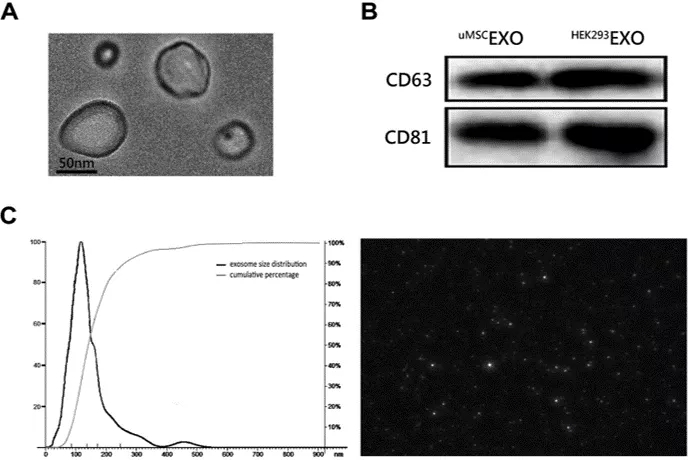
1. 外泌体为表面不规则、有明显生物膜结构的球形结构;
2. 外泌体特异性标记物CD63和CD81的表达;
3. 外泌体平均直径60-120nm。
2.HA凝胶的表征及其外泌体保留能力
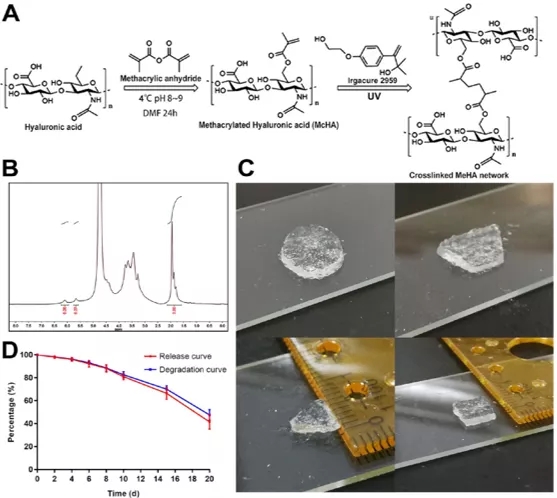
1. HA骨架中,甲基丙烯酸酯基团的修饰密度约为30%;
2. HA凝胶在紫外下30min后可塑造成任何形状;
3. 在PBS中浸泡20天后,还有约40%的外泌体仍停留在HA凝胶内。
3.三维多孔nHP支架的观察与表征

1. 支架为直径5mm,1.5mm的圆柱形,支架内约300µm大的空隙结构互相连接;
2. 构建凝胶/nHP复合材料,空隙结构中充满了交联水凝胶。
二、uMSCEXOs在体内和体外的修复作用
1.uMSCEXOs促进了体内颅骨缺损的修复
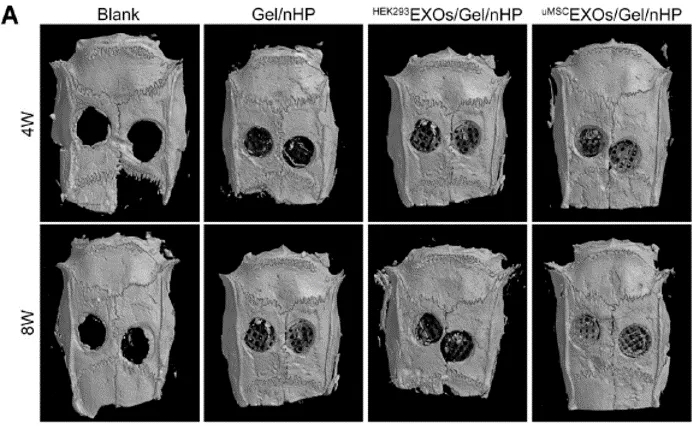
大鼠颅骨损伤第四周和第八周时的纤维CT三维重建图显示uMSCEXOs/Gel/nHP组中胶原生长显著增加。
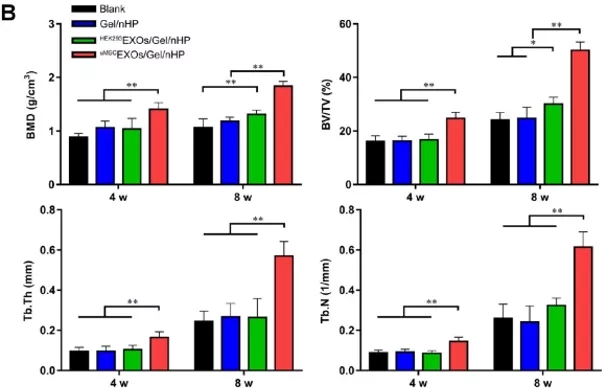
BMD、BV/TV、Tb.Th、Tb.N定量分析显示uMSCEXOs组中颅骨缺损修复情况良好。
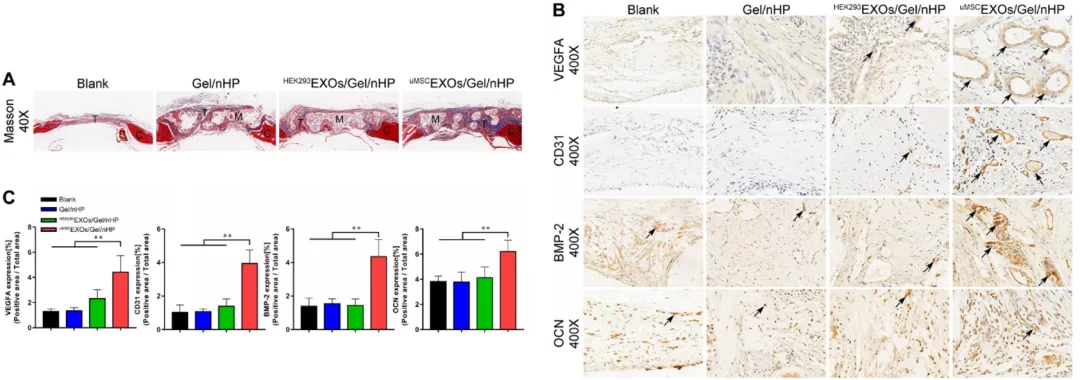
1. uMSCEXOs组支架内形成了大量的骨样基质和胶原;
2. 免疫组化显示uMSCEXOs组中骨再生相关因子VEGFA、CD31、BMP-2和OCN的相关阳性细胞区域比其他组的大;PCR定量结果与IHC结果一致, uMSCEXOs组中相关因子的表达明显高于其他组。
2.uMSCEXOs的体外促血管生成和促成骨作用
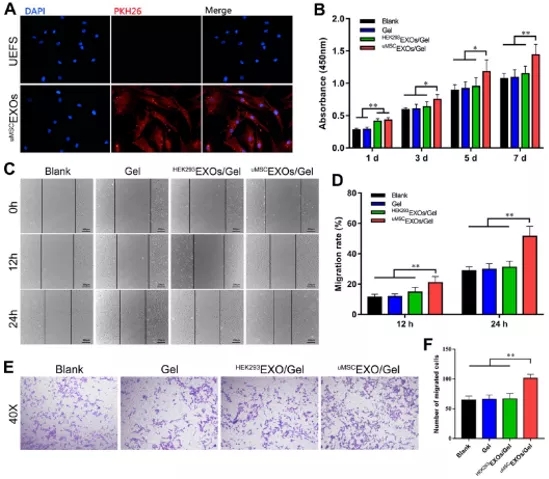
1.血管生成实验,根据血管总长度和管状结构的完整度, uMSCEXOs 组细胞的血管形成能力更强;
2.RT-PCR结果表明, uMSCEXOs 组中促血管生成的相关基因表达水平升高。
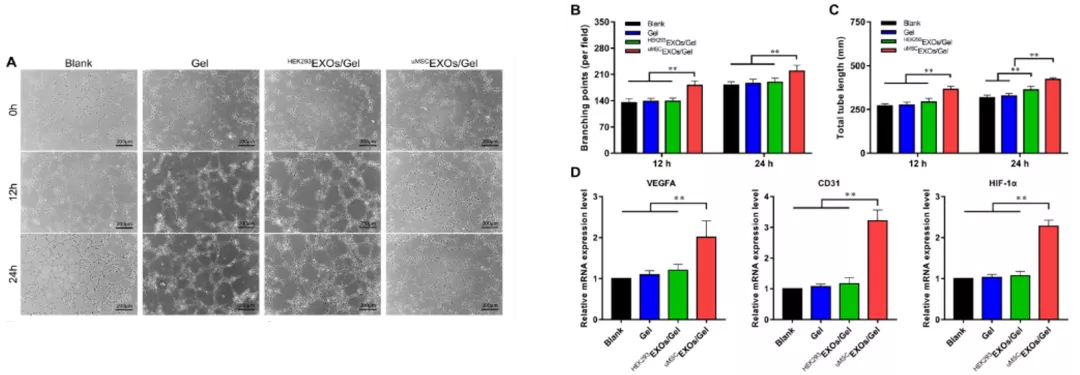
1.血管生成实验,根据血管总长度和管状结构的完整度, uMSCEXOs 组细胞的血管形成能力更强;
2.RT-PCR结果表明, uMSCEXOs 组中促血管生成的相关基因表达水平升高。
小结:uMSCEXOs在体内能够促进颅骨缺损修复,在体外具有良好的促血管生成作用。
三、验证uMSCEXOs的修复作用
1. uMSCEXOs中miR-21含量丰富
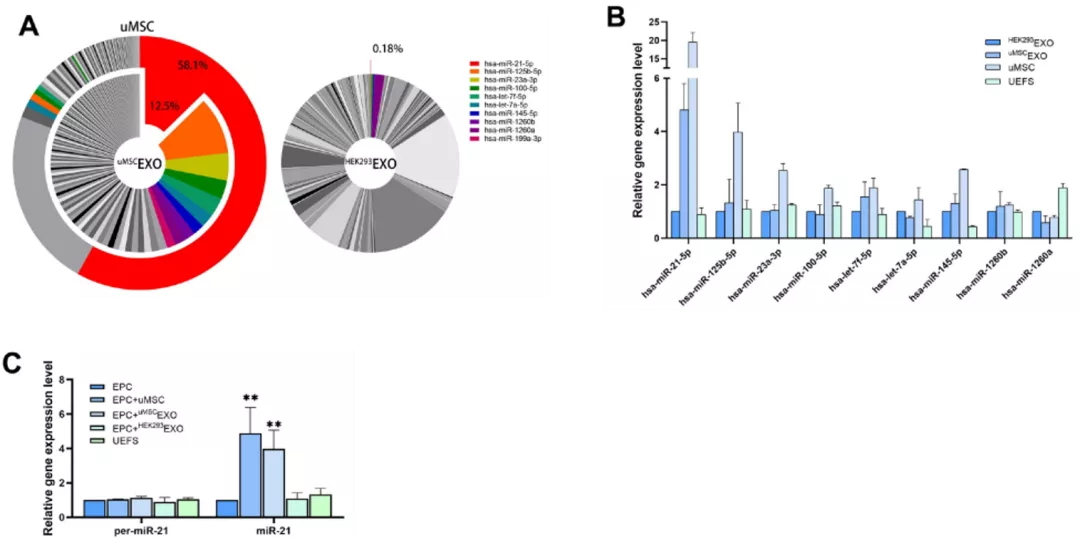
1.在uMSCEXOs含量最丰富的miRNA中,只有miR-21在uMSC中也高表达,PCR验证结果与高通量测序结果一致;
2.RT-PCR检测经不同处理后的EPCs中的miR-21表达水平,uMSC和uMSCEXOs 组中的miR-21表达明显高于其他两组。
(注: uMSCEXOs显著提高了EPCs中成熟miR-21的水平,但不影响miR-21前体的水平,排除了外泌体诱导EPCs内源性miR-21表达的可能性。)
2. uMSCEXOs中miR-21在体内和体外均能促进血管生成
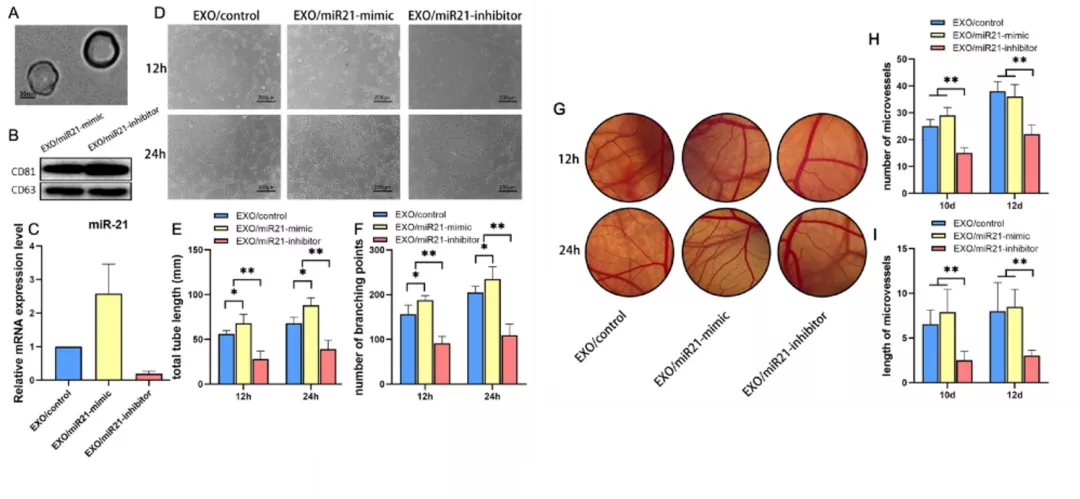
改变miR-21的水平,验证uMSC来源的外泌体miR-21的作用:
1.用miR-21表达水平不同的外泌体处理EPCs细胞,血管生成实验表明miR-21的含量变化对血管生成有明显的影响;
2.鸡胚CAM实验表明,上调uMSCEXOs中miR-21的表达水平,促进了CAM中的血管生成作用。
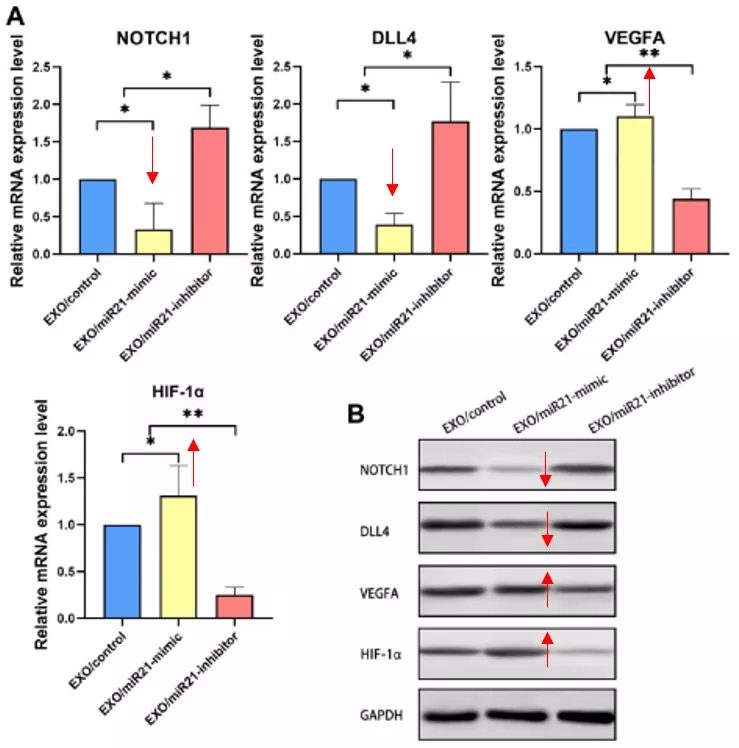
NOTCH信号通路是控制血管生长、分化和正常血管发育的一个高度保守的关键通路,它通过DLL4负调控VEGFA信号通过的受体VEGFR2的表达。
结果:uMSCEXOs能够降低EPCs细胞中NOTCH1和DLL4的表达水平,升高VEGFA和HIF-1α的表达水平。
总结与思考
研究首次揭示了NOTCH1/DLL4通路在外泌体mir-21诱导的血管生成中发挥重要作用。外泌体miR-21被确定为一种细胞间信使,通过抑制NOTCH1/DLL4通路,诱导VEGFA和HIF-1α的表达来增强血管生成,从而促进骨损伤修复。
文献中涉及的实验技术
以上文献涉及的实验技术,均可在晶莱生物展开。
【晶莱生物】是一家专注于生物医学领域内科研学术服务的高新技术企业,致力于打造国内一流的生物技术服务品牌。为生物医学研究者提供动物造模、细胞生物学、基因组学、蛋白鉴定及分析、病理组化、表观遗传学等多个实验平台服务。


