
肝纤维化是一种慢性肝病在修复过程中的病理状态,其中慢性肝病包括慢性病毒性肝炎、酒精性肝病、非酒精性脂肪性肝炎、胆汁淤积性肝炎以及某些代谢性疾病等。
研究表明,肝纤维化作为所有慢性肝病的共同病理阶段,是肝硬化甚至肝癌发展的必经阶段。大量研究证明,适当的治疗措施可逆转肝纤维化和早期肝硬化病理状态,控制肝纤维化的发展对于肝硬化甚至肝癌的防治具有至关重要的作用。因此,逆转肝纤维化的治疗成为众多慢性肝脏疾病治疗的汇聚点。
而制造各致病因素动物模型是深入研究肝纤维化发病机制及治疗药物的前提基础。
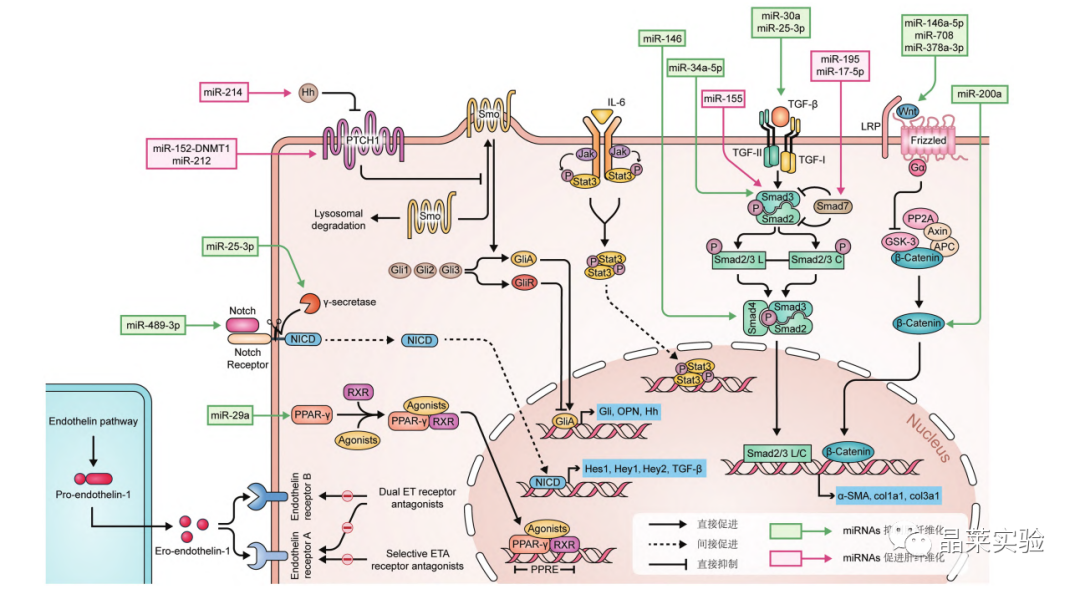
肝纤维化信号传导通路图
1.四氯化碳诱导肝纤维化模型
四氯化碳法诱导肝纤维化模型的原理属于氧化应激反应,机制是四氯化碳在肝脏内代谢生成三氯甲基自由基,产生的自由基诱发脂质过氧化反应,生成的过氧化物包括丙二醛和4-羟基壬烯酸,它们以线粒体为靶点,破坏线粒体膜结构,从而损伤肝细胞膜,激活肝星状细胞(hepaticstellatecell,HSC)释放Ⅰ型胶原酶和Ⅳ型胶原酶,促进HSC增生,导致肝纤维化。
目前常用的四氯化碳造模法主要包括腹腔注射、皮下注射及灌胃法。
造模方法:
皮下注射浓度为40%~60%的四氯化碳联合橄榄油是最常用的造模方法,每周注射2~3次,第8周时可成功制造肝纤维化模型。
2. 二甲基亚硝胺诱导肝纤维化模型
二甲基亚硝胺(dimethylnitrosamine,DMN)也叫亚硝基二甲胺,具有巨大的肝毒性,对基因结构及免疫功能也具有一定的损伤作用。
其主要作用机制是使核酸、蛋白质发生甲基化,大剂量使用易导致动物死亡,多次小剂量腹腔注射、灌胃及吸入可以导致肝细胞坏死,细胞外基质增多致使HSC被激活,细胞表型由上皮型转化成间质型,促使HSC转化成纤维细胞,导致肝脏退行性坏死,形成肝纤维化。
造模方法:
大鼠1.6mL/kgDMN溶液腹腔注射,3次/周,42d时大鼠出现明显的肝纤维化,即肝小叶消失、假小叶形成。
腹腔注射质量分数0.5%DMN溶液2mL/kg,每2d注射1次,连续4周,得到稳定的肝纤维化模型。
3. 硫代乙酰胺诱导肝纤维化模型
硫代乙酰胺(thioacetamide,TAA)分子式为CH3CSNH2,其诱导的急性肝损伤机制是TAA进入细胞内,被细胞色素氧化酶P450氧化后生成自由基,自由基与肝细胞膜脂质结合,诱发脂质过氧化破坏肝细胞膜,造成肝细胞的变性坏死。
主要的造模方法有灌胃、腹腔注射、皮下注射等,最常用的是皮下注射。
造模方法:
灭菌注射用水将TAA配制成质量浓度为40mg/mL的溶液,对大鼠进行腹腔注射,3次/周,第8周时肝纤维化模型造模成功。
大鼠皮下注射0.03%的TAA,剂量为200mg/kg,2次/周,8周时肝纤维化模型造模成功。
酒精分子式为C2H6O,进入人体内的酒精有90%在肝脏中代谢,其肝损伤机制是酒精进入肝脏细胞,在脱氢酶和微粒体乙醇氧化酶系的作用下转化为乙醛,进而转变为乙酸,促使还原性辅酶Ⅰ与反应性辅酶Ⅰ比值升高,抑制线粒体三羧酸循环,使肝内脂肪酸代谢发生障碍,氧化减弱,使中性脂肪堆积于肝细胞中,从而引起肝细胞的炎症、变性、坏死,诱发胶原纤维堆积导致肝纤维化。
造模方法:
目前主要通过31.5%酒精溶液(95%酒精与水混合制成)灌胃的方法制备酒精性肝纤维化模型。
采用“白酒-吡唑-植物油”混合液灌胃法制备乙醇肝纤维化动物模型,即每天给予每只大鼠以4.8g/kg白酒、24mg/kg吡唑、2mL/kg玉米油的混合液灌胃,灌胃量随体重的变化进行调整,同时喂养高脂饲料(基础饲料∶胆固醇∶猪油=79∶1∶20),于16周时发现大鼠轻度酒精性肝纤维化形成。
1. 蛋氨酸和胆碱缺乏(methionineandcholinedeficient,MCD)饲料目前常用MCD饲料构建研究非酒精性脂肪性肝炎模型。
MCD模型在脂肪性肝纤维化研究中很常见。胆碱、蛋氨酸均缺乏时,谷胱甘肽和卵磷脂合成受阻,导致VLDL合成及分泌障碍,造成TG在肝细胞沉积,并增加抗氧化屏障机制损伤导致氧化应激加剧,肝细胞发生炎症和坏死。
然而这种饮食模式构建的动物模型缺乏一些人类患者的主要病理特征,如无血清胰岛素、空腹血糖、瘦素和甘油三酯等水平降低。目前常采用复合造模的方式以改善上述不足,在MCD饲料的基础上结合基因修饰小鼠,能更好地模拟人类肝纤维化特点。
2. 高脂类饲料
高脂高胆固醇所致肝纤维化的主要机制是:肝脏是脂肪代谢的重要场所,它可把血液中的脂肪酸合成为三酰甘油,三酰甘油与载脂蛋白结合为脂蛋白,并释放入血液;长期摄入过多的动物脂肪、植物油和糖类等高热量食物,过剩的营养物质在体内不能被充分利用,从而转化为脂肪储存起来,导致脂肪肝,肝脏的细胞“堆”满了多余的脂肪,从而形成肝纤维化。
胆管结扎性肝纤维化模型是通过人为结扎肝外胆管使其阻塞,形成肝纤维化。
其结扎方法包括肝外胆管结扎法、胆管结扎后切断法和逆行性注入N-丁基-2-氰基丙烯酸盐法三种方式。
其主要机制是由胆管渐进性破坏、胆汁淤积及肝内炎症持续存在,导致肝细胞及胆管细胞进一步损伤,发展为肝纤维化。
肝缺血再灌注损伤(Hepaticischemia-reperfusioninjury,HIRI)诱导的肝纤维化模型。
HIRI是指肝缺血再灌注后,不仅不会恢复肝功能,反而让肝结构和功能损害更严重的现象。在临床上严重肝外伤、肝移植、休克复苏时均不可避免出现HIRI,利用HIRI这一操作形成的一种新型肝纤维化模型,既符合临床实际,也为这方面的研究提供一种新的方向。
肝细胞损伤后释放炎症因子、细胞因子和自由基促使HSC被大量激活而启动早期肝纤维化。
自身免疫性肝纤维化的发病机制主要以遗传因素为主,其他因素是在遗传易感性基础上,导致机体免疫耐受机制破坏,从而产生针对肝脏自身抗原的免疫反应,诱发肝脏炎症坏死并进展为肝纤维化。
实验研究中主要以动物血清或者人血清蛋白作为抗原,将其注射入动物体内,复制肝纤维化动物模型。
1. 动物血清诱发的肝纤维化模型
实验室一般常选用猪血清、牛血清、马血清或血吸虫血清等给予实验动物注射,引起胶原纤维堆积,导致肝小叶消失,形成假小叶,诱发肝纤维化。
由于猪血清较牛血清价格便宜,而血吸虫血清不易提取、价格昂贵,因此猪血清是实验室肝纤维化造模的首选试剂。
造模方法:
采用猪血清(0.5mL/次,2次/周,共12周)对大鼠进行腹部注射,在造模期间每周处死1只大鼠,观察胶原纤维、肝纤维化指标及转化生长因子β1,用来判断大鼠成模情况,结果显示,猪血清可成功诱导肝纤维化模型。
在传统猪血清诱导肝纤维化(腹腔注射,0.5mL/次,共12周)的基础上进行改良,加用高脂高胆固醇饲料(80%玉米粉+20%猪大油+0.5%的胆固醇)饲养大鼠,结果发现实验第4周时大鼠出现肝纤维化的现象。
2. 人血白蛋白诱发的肝纤维化模型
人血白蛋白所致的肝纤维化分为致敏和攻击两个阶段。
使用生理盐水稀释人血白蛋白,与等量的不完全福氏佐乳剂乳化,予尾静脉注射0.5mL/次(含人血白蛋白4mg),共注射4次,前2次间隔14d,后2次间隔10d,并以30%乙醇为唯一饮用水,结果显示苏木精-伊红染色、V-G胶原染色向肝小叶延伸,交织成网状;进一步研究发现,在攻击阶段由尾静脉注射改为腹腔注射,或者在注射人血白蛋白的基础上加用四氯化碳,可增加造模成功率。
3. 刀豆素蛋白诱发的肝纤维化模型
刀豆素蛋白诱导肝纤维化的机制是刺激T细胞有丝分裂,促进细胞因子(转化生长因子β、肿瘤坏死因子α等)的释放,引起炎症反应,进一步使肝炎发展成肝纤维化。
研究表明将1g/L刀豆素蛋白溶于灭菌的磷酸盐缓冲溶液,按12.5mg/kg给予每只大鼠进行尾静脉注射,1次/周,第6次注射1周后处死大鼠,取肝组织分析。发现刀豆素蛋白诱导的大鼠肝纤维化与人类肝炎病毒肝纤维化接近,随着刀豆素蛋白剂量的增加,肝损伤加重。
综上所述,猪血清诱导肝纤维化模型是免疫性肝纤维化模型中最为经典的模型,其操作简单、价格便宜、造模周期短,与化学药物诱导的肝纤维化模型相比,稳定性更高,与临床肝纤维化最为贴近,可以更好地服务于临床基础研究。
乙型肝炎病毒(HBV)和丙型肝炎病毒(HCV)与宿主之间的相互作用复杂,除非病毒被宿主清除,否则宿主将长期携带病毒,肝损害无法愈合最终会导致纤维化、硬化甚至癌症的发生。
HCV感染以及其他可能的人类肝病性病原体实验提供实验可能性,并证明可测试抗病毒药物。
基因遗传因素是肝纤维化中一个重要影响因素,构建小鼠转基因肝纤维化模型包括基因敲除、基因突变和基因转染等方法,通过一条明确的途径来研究肝纤维化的发病机制。
基本步骤是将裸质粒DNA大量高速注射到动物尾静脉,该方法实现了肝中外源基因的高表达,为实验动物提供了一种高效简单的转染方法。
基于流体动力学的基因传递系统建立了动态小鼠肝纤维化模型,发现小鼠肝中的TGF-β可高水平表达,在诱导状态下Col1A2和血清α-SMA这两个纤维化和HSC活化的指标上调。
这种模型代表了一种动态且可逆的肝纤维化,可用来研究肝纤维生成的早期分子机制或筛选用于临床的抗纤维化药物。
其他基因模型还有Ob/ob、Db/db、Foz/Foz、SREBP-1c转基因等。
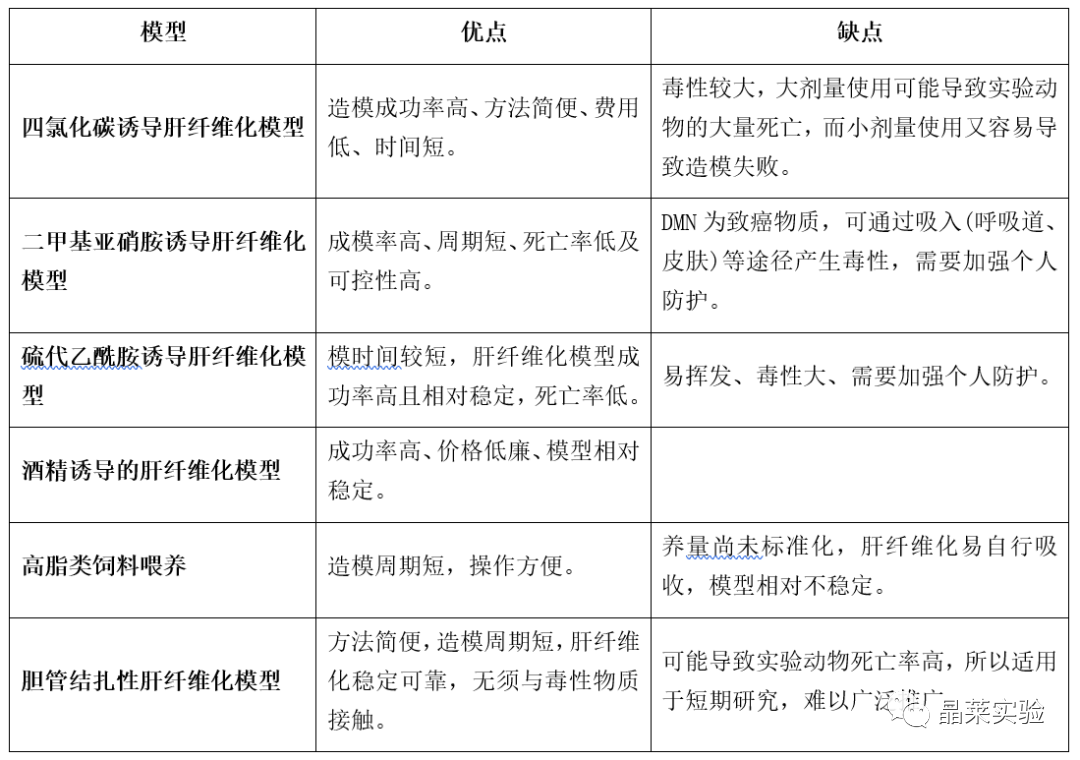
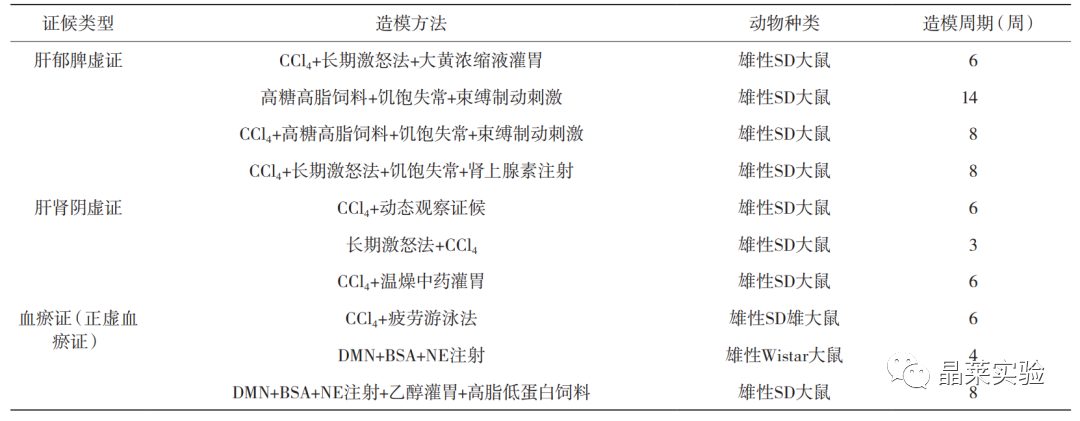
1. 常见HF病证结合动物模型总结
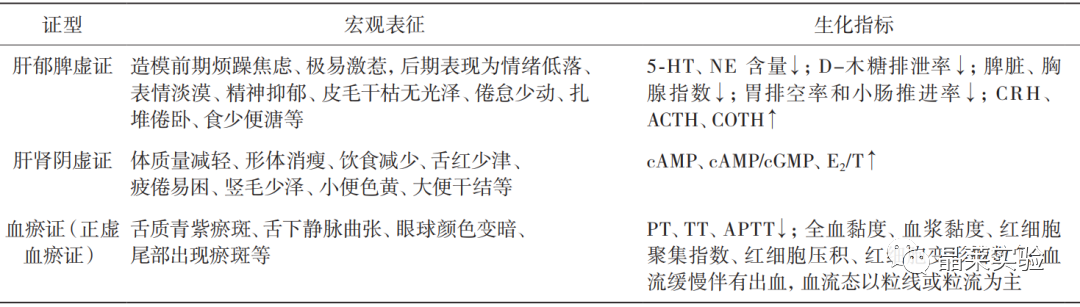
2. HF病证结合动物模型证候特征评价方法
关注公众号,了解更多动物模型技巧!
