

2024年1月4日,新加坡研究学者在期刊CellStem Cell(IF:23.9003)发表 了 - 篇 题 为J“Kidney organoidcilium-autophagymodels revealmetabolic axis as atherapeutictarget for PKD both in vitro and invivo”的文章。
该文主要讨论了利用人类多功能干细胞来源的肾脏类器官模型(organoids)来研究多囊肾病(PKD)的潜力。多囊肾病是一种遗传性疾病,目前还没有有效的治疗方法。
研究团队开发了两种关键模型以深入探索多囊肾病的机制:一种是体外(in vitro)肾脏类器官模型,另一种是体内(in vivo)模型。这两种模型均展现出肾脏损伤以及肾素-血管紧张素醛固酮系统的异常上调现象。
团队通过单细胞分析技术,揭示了囊性变过程中发生的多种代谢变化,其中特别指出了自噬过程出现的缺陷。自噬作为一种至关重要的细胞内机制,负责物质的降解与循环利用,对于维持细胞稳态具有不可替代的作用。
在实验中,研究团队尝试通过不同手段激活自噬过程,观察其对多囊肾病囊性变的影响。他们发现,无论是通过过表达ATG5基因还是消除初级纤毛,都能显著抑制囊性变的进展。
此外,研究团队还利用了一种特殊的肾脏类器官异种移植模型,该模型能够自发地发展出肾小管囊肿,从而更加真实地模拟了多囊肾病的病理过程。在这一模型中,他们测试了一种名为米诺地尔的强效自噬激活剂。结果显示,米诺地尔能够有效地抑制囊肿的形成。
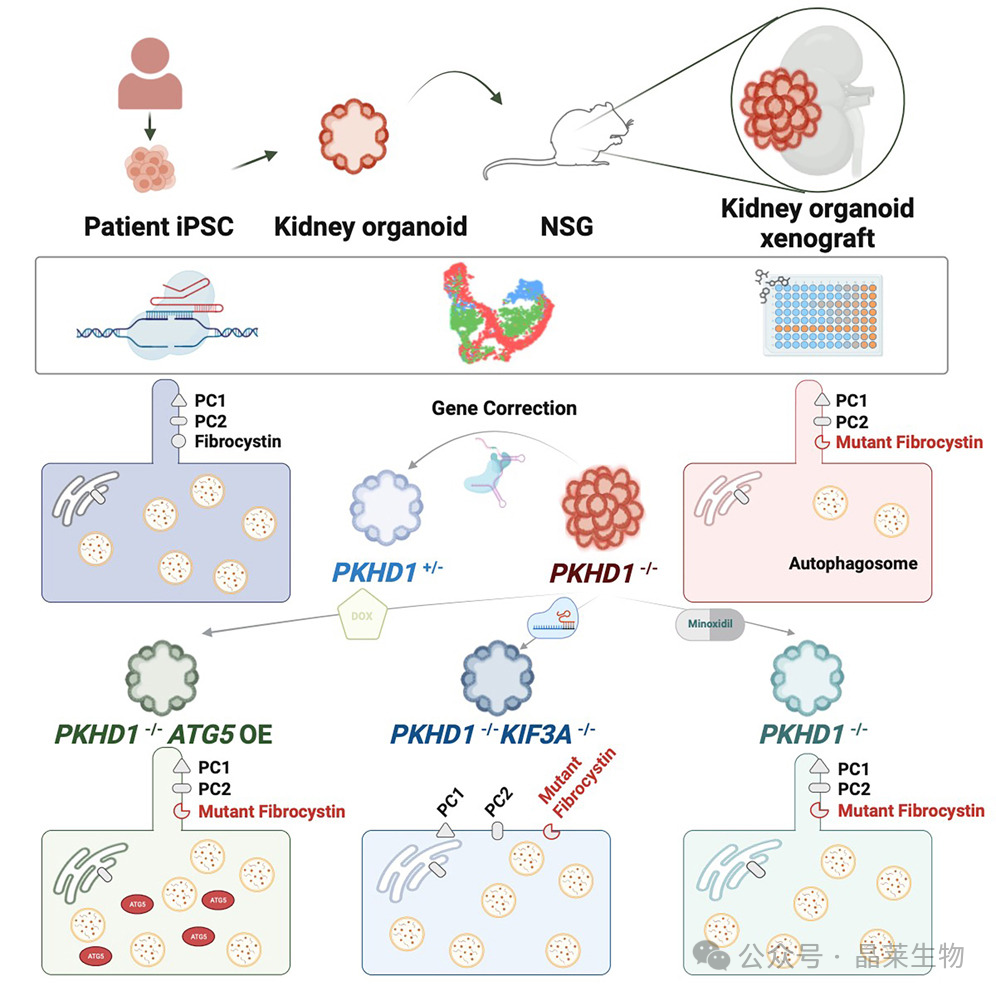
1.建立人类多功能干细胞(hPSC)来源的肾脏类器官模型,作为研究PKD的模型系统。
2.描述类器官模型中PKD的关键特征,如囊肿形成和细胞代谢紊乱。
3.研究涉及PKD的代谢和细胞过程,包括纤毛-自噬代谢轴。
4.利用各种实验技术评估靶向纤毛-自代谢轴在PKD中的治疗潜力,如酶联免疫吸附试验(ELISA)、生物化学分析和Western印迹。
5.利用先进的成像技术量化自噬体的形成和囊肿指数分析。
6.在NSG小鼠体内利用器官移植模型评估潜在治疗干预的有效性。
7.对疾病机制进行全面的分子和细胞表征。
8.确定PKD治疗的新途径。
1. 在多囊肾病肾脏类器官中,紊乱的cAMP代谢和钙离子稳态是囊肿形成的机制
在多囊肾病肾脏类器官中,囊肿的形成与紊乱的cAMP代谢和钙离子稳态密切相关。研究显示,细胞内钙信号传导的紊乱抑制了磷酸二酯酶1/3(PDE1/3)对cAMP的水解作用,同时增强了AC6对cAMP的合成。这一变化导致细胞内cAMP水平显著升高,进而促进了囊肿的形成。此外,硝地平作为一种强效的L型钙通道阻滞剂,能够诱导多囊肾病肾脏类器官形成囊肿,并伴随细胞内cAMP水平的升高。
2. 多囊肾病肾脏类器官表现出肾小管损伤和异常的肾素-血管紧张素醛固酮系统(RAAS)激活
多囊肾病肾脏类器官还表现出肾小管损伤和肾素-血管紧张素醛固酮系统(RAAS)的异常激活。无论是常染色体显性多囊肾病(ADPKD)还是常染色体隐性多囊肾病(ARPKD)的肾脏类器官,都在近端和远端小管中形成了囊肿,且囊肿的严重程度与细胞内cAMP水平呈正相关。同时,这些肾脏类器官在体内和体外均表现出RAAS的异常激活,这与多囊肾病患者的临床表现相一致。
3. 单细胞多组学测序揭示了PKD肾脏类器官中多种代谢变化
利用单细胞多组学测序技术,研究人员深入探讨了PKD肾脏类器官中囊肿形成过程中的代谢变化。通过在单细胞水平上分析基因表达和染色质可及性,该研究确定了多种在PKD肾脏类器官囊肿形成过程中发生的代谢变化。
4. 通过遗传靶向干预纤毛-自噬代谢轴可消除囊肿形成
通过遗传手段靶向干预纤毛-自噬代谢轴,可以有效抑制PKD肾脏类器官中的囊肿形成。研究证明,自噬作为囊肿形成的关键调控机制,其激活对于抑制囊肿至关重要。通过过表达ATG5(自噬体形成的关键调节因子)来刺激自噬,可以显著抑制常染色体隐性多囊肾病(ARPKD)肾脏类器官中的囊肿形成。此外,主要纤毛的消融也被证实能显著抑制PKD肾脏类器官中的囊肿生长,这凸显了纤毛与自噬在PKD发病机制中的复杂且重要的相互作用。
5. 候选药物通过上调自噬抑制囊肿形成
研究团队发现了几种化合物和药物,它们能够显著降低PKD肾脏类器官的囊性指数,同时保持肾小管样结构和血管网络的完整性,并减少KIM1的表达。在这些药物中,2-脱氧-D-葡萄糖(2-DG)、甲福明(metformin)和雷帕霉素(rapamycin)因具有诱导自噬的能力而备受关注。此外,米诺地尔(minoxidil)作为一种有效的自噬激活剂,且已获得美国食品药品监督管理局(FDA)批准,其在体内实验中也被证实能有效抑制类器官异种移植模型中的囊肿形成。
6. PKD类器官异种移植模型在体内自发形成囊肿
研究团队采用了PKD类器官异种移植模型。该模型通过将ARPKD患者诱导多能干细胞(iPSC)和基因纠正的iPSC衍生的肾脏类器官植入免疫功能低下的NOD scid gamma(NSG)小鼠的肾下包膜空间来构建。移植后四周,ARPKD和基因纠正的肾脏类器官均成功与宿主循环系统吻合,这通过异种移植中肾小球灌注得到证实。值得注意的是,ARPKD肾脏类器官的异种移植自发形成了管状囊肿,而基因纠正的类器官异种移植则未发生囊肿,这进一步验证了PKD的发病机制。
7. 遗传和药理学刺激自噬抑制PKD肾脏类器官异种移植模型中的体内囊肿形成
该研究发现遗传和药理学刺激自噬均抑制了PKD肾脏类器官异种移植模型中的体内囊肿形成。具体来说,研究人员在ARPKD肾脏类器官中过表达了ATG5(自体聚集的关键调节因子),并通过全身DOX给药诱导宿主NSG小鼠中的ATG5过表达。
结果显示,DOX以剂量依赖的方式显著抑制了ARPKD肾脏类器官异种移植模型中的囊肿形成,支持自噬在体内囊肿形成中发挥保护作用。
本研究开发了一种体外和体内类器官模型,用于研究多囊肾病(PKD),该模型再现了关键的PKD疾病表型,包括肾小管损伤和肾素-血管紧张素醛固酮系统异常上调。研究发现了在囊性病变过程中发生的多种代谢变化,包括自功能受损。研究证实,自在囊性病变过程中起着主要的作用,通过过表达ATG5或切除初级纤毛可以抑制PKD类器官中的囊肿形成。研究还发现了几种化合物和药物,通过上调自显著降低了PKD类器官的囊性指数。
体内类器官异种移植模型为研究PKD的发病机制和评估潜在的治疗方法提供了有价值的工具。
参考文献:
Kidney organoid models reveal cilium-autophagy metabolic axis as a therapeutic target for PKDboth in vitro and in vivo.Cell stem Cell.2024 Jan 4;31(1):52-70.e8. doi.10.1016/j.stem.2023.12.003.PMID: 38181751.
关于晶莱
