

肺类器官作为先进的三维(3D)细胞培养模型,在探索人类肺部发育机制及呼吸道疾病的研究中发挥着关键作用。这些疾病涵盖广泛,如SARS-CoV、H1N1、MERS等病毒感染,囊性纤维化、哮喘/慢性阻塞性肺疾病(COPD),以及空气污染和吸烟对健康的影响。与传统方法如使用永生化肺细胞系或原代细胞相比,肺类器官的优势在于其包含了多种分化的细胞类型,并模拟了体内复杂的组织结构,从而提供了更为接近真实生理环境的模型。
肺类器官能从有限的患者组织样本或多能干细胞中衍生出来,这为个性化生物医学研究建立了宝贵的活体生物库。其中,3dGRO™人肺类器官培养系统是一个高效、无血清且多阶段的方案,它能够将人诱导多能干细胞(iPS)成功分化为成熟的肺类器官,这些类器官的结构与体内的分支气道和早期肺泡结构高度相似。
通过3dGRO™系统生成的肺类器官不仅数量可观,而且表达了多种标志物,这些标志物是成熟肺和气道中各种细胞类型的特征,例如II型肺泡上皮(ATII)细胞中的SFTPB和SFTPC(表面活性物质相关蛋白B和C),气道杯状细胞中的MUC5AC,以及肺内胚层标记EpCAM、Sox9和Nkx2.1,纤毛细胞中的乙酰-α-微管蛋白,还有间充质标记波形纤维蛋白。
此外,肺类器官还具备表达血管紧张素转换酶2 (ACE2) 和TMPRSS2的能力,这两种分子分别作为SARS-CoV-2病毒(导致COVID-19的病原体)的受体和辅助其入侵的丝氨酸蛋白酶,使得肺类器官成为研究新型冠状病毒及其感染机制的重要工具。综上所述,肺类器官及其培养系统为研究肺部生理、病理过程以及开发针对呼吸道疾病的新疗法提供了强有力的支持。
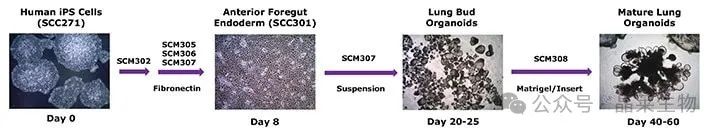
人肺类器官分化实验流程
使用诱导培养基(SCM302)在4天内将人多能干细胞分化成定型内胚层细胞。在第4-8天,诱导培养基 (SCM305、SCM306) 将人定型内胚层细胞分化为前肠内胚层 (AFE)。AFE细胞可以冷冻保存 (商业化产品货号SCC301) 或使用 3dGRO™ 肺类器官分支培养基 (SCM307) 进一步分化成分支肺芽型类器官,并使用 3dGRO™ 肺类器官成熟培养基 (SCM308) 进一步成熟为分支型和肺泡型类器官。
1. 人 iPS 细胞分化为定型内胚层( 0-4 Day)

注意:从高品质未分化的人 ES/iPS 细胞 (SCC271) 开始,这些细胞汇合度约为 70-80%,且含有 <5% 的分化细胞。以下方案用于六孔组织培养处理板中的一孔。指示的体积针对单孔。请根据需要调整用量。
2. DE 细胞分化为前肠内胚层细胞(4-8 Day)

注意:在定型内胚层细胞的第 4 天和分化为前肠内胚层 (AFE) 细胞后的第 8 天,应观察到较高细胞密度。下面的方案提供了 6 孔板型的参考接种密度。其他板型的接种密度需做调整。

类器官处于悬浮培养中,根据方案进行培养基更换:
① 使用1mL玻璃血清移液器将漂浮的类器官转移到无菌的15mL锥形管中。等待10分钟,使类器官沉淀到试管底部。
② 将2mL吸液管连接真空泵。在2mL吸气移液器上,连接一个无菌的20μL非屏障移液器枪头。小心地吸出培养基。注意在类器官上方留下少量培养基作为缓冲液,以避免干扰类器官。
③ 将0.5mL3dGRO™肺类器官分支培养基(SCM307)添加到含有类器官沉淀的15mL管中。用1mL玻璃移液器上下吹打两次。将类器官转移回超低附着24孔板中的同一孔中。
④ 将0.5mL3dGRO™肺类器官分支培养基(SCM307)添加到15mL锥形管中,冲洗并收集所有剩余的类器官。将冲洗液添加到超低附着24孔板的同一孔中。总体积=每孔1mL。
4. 将肺芽类器官 (LBO) 分化为成熟的肺类器官( 25-60Day )

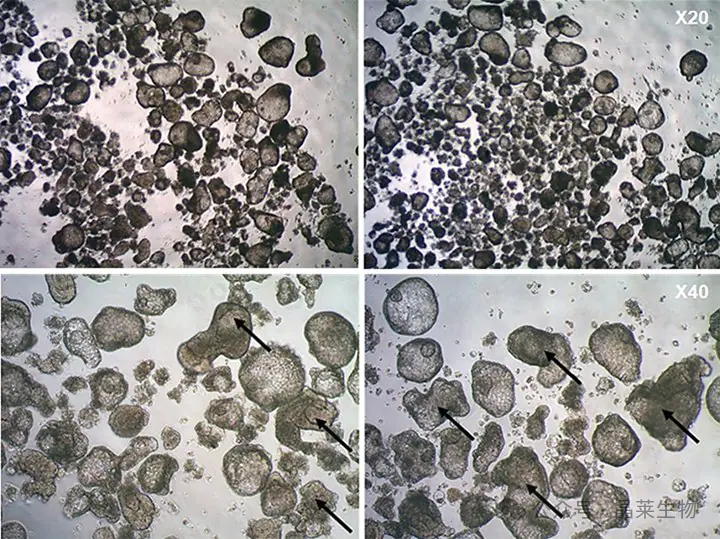
悬浮培养的人肺芽类器官(LBO)
分化第23天未成熟人iPS细胞衍生LBO的形态学
注意:培养至20-25 天,会有许多漂浮的肺类器官。每个 ECM基质胶 包埋夹层应包含大约 4-6 个类器官。根据您计划制作的 ECM基质胶包埋夹层的数量,计算96 孔板中制备类器官/ECM基质胶悬浮液所需的孔总数。
1. 肺类器官成熟的时间过程
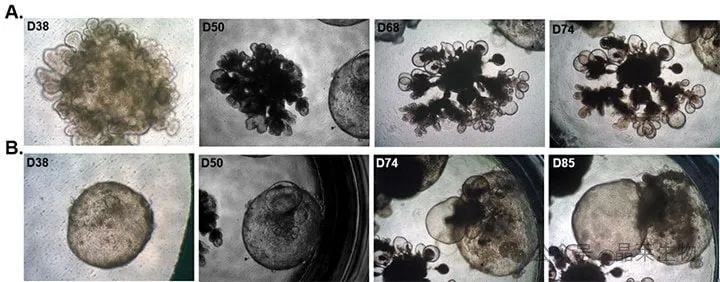
在两个单独的孔中追踪人iPS 细胞衍生的肺类器官分化
在第20至25天的时间窗口内,选取大约4至6个未成熟的肺芽(LBO),并将它们嵌入到细胞外基质(ECM)基质胶中。采用3dGRO™肺类器官成熟培养基来支持这些肺类器官的发育。
在培养过程中,观察到多种形态变化。其中,一些肺类器官在顶端区域形成了分支结构,这些结构可能代表了肺部的气道系统。同时,还有一些肺类器官呈现出圆形扩张的形态,其中心区域则发育出了类似于肺泡球的致密组织,这可能与肺部的气体交换功能相关。
随着培养时间的延长,当这些肺类器官持续培养超过60至70天时,一些较大的圆形结构出现了破裂现象。这些结构的破裂伴随着粘液样物质的释放。
2. 肺类器官标记表达
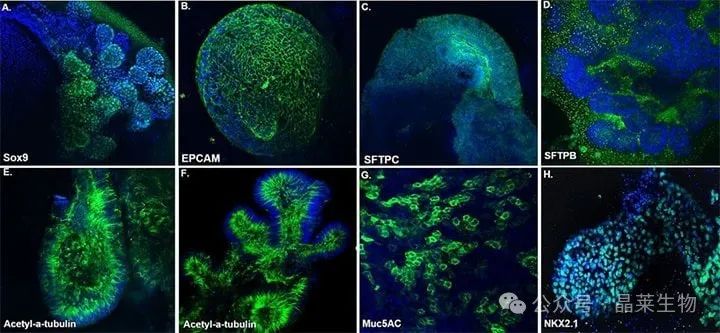
在第70天,对人外周血单核细胞(PBMC)来源以及人肺成纤维细胞(HFF)衍生的诱导多能干细胞(iPS细胞)所形成的成熟肺类器官进行了标志物的表达分析。
II型肺泡上皮细胞,这类细胞负责产生表面活性物质,以维持肺泡的稳定性,通过表达表面活性物质相关蛋白SFTPC和SFTPB得到了确认。同时,气道杯状细胞,其特征是分泌粘液以保护气道,通过表达Muc5AC标志物得到了验证。
此外,肺内胚层细胞,这是肺部发育过程中的关键细胞类型,通过表达EPCAM(上皮细胞粘附分子)、Sox9(一种转录因子,对肺部发育至关重要)和NKX2.1(一种与肺和甲状腺发育相关的同源框基因)等标志物得到了识别。
纤毛细胞,这类细胞具有运动纤毛,有助于清除气道中的异物和病原体,通过表达Acetyl-α-Tubulin(乙酰化α-微管蛋白,纤毛的主要结构成分)得到了确认。

关于晶莱
