

在药物研发的过程中,候选药物的评估是一个系统而严谨的过程,每一步都旨在确保药物的安全性和有效性。针对候选药物在体外表现出较好的抗肿瘤活性后的一系列步骤,我们可以进行以下详细分析:
① 体外实验的重要性不容忽视。在这一阶段,利用细胞培养等技术在实验室环境中测试候选药物对肿瘤细胞的抑制或杀灭效果。这些实验通常可以快速筛选出具有潜在抗肿瘤活性的化合物,为后续研究提供方向。
② 体外实验的结果并不能直接应用于人体。因为人体内的环境远比实验室中的细胞培养环境复杂得多,涉及多种细胞类型、组织结构和生理功能的相互作用。因此,当候选药物在体外实验中表现出良好的抗肿瘤活性时,这只是药物研发过程中的一个初步积极信号。
③ 为了验证药物在人体内的潜在疗效和安全性,候选药物需要被推进到体内抗肿瘤实验,即临床前有效性研究。这一阶段通常包括动物实验,如小鼠或大鼠模型,以模拟人体内的肿瘤生长和药物反应。这些实验旨在评估药物在生物体内的吸收、分布、代谢、排泄(ADME)特性,以及其对肿瘤生长的抑制作用和对正常组织的潜在毒性。
临床前研究的结果对于决定是否将药物推进到临床试验阶段至关重要。如果候选药物在动物模型中表现出显著的抗肿瘤效果且毒性可控,那么它就有可能被选为进入临床试验的候选药物。
1. 材料
细胞、药物
2. 实验内容
药物最佳浓度选择/最佳时间点(24 48 72)
分组:(n≥3,3/5)
① 对照组
② 给药组(6个以上浓度梯度)(基于文献设计浓度梯度)
检测:CCK8检测/MTT检测
3. 药物效果研究
分组(n=3,1个时间点)
① 对照组
②给药组(高中低3个剂量;或者最佳药物浓度及时间点)
检测:增殖CCK8、侵袭、迁移、克隆形成、血管形成等----细胞表型验证。
多种参数用于评价候选药物的抗肿瘤活性,包括有肿瘤体积、动物体重、实验结束时的肿瘤重量以及肿瘤图片【将小鼠处死后摆放并拍整鼠(带瘤子)照片或将剥离瘤块摆放拍照,来表现治疗效果】。
1. 材料:荷瘤
① 细胞:
② 动物:品系选择要对应细胞系
③ 药物:候选药物
2. 实验内容 分组:(n≥3)
① 对照组
② 给药组(高中低3个剂量;或者最佳药物浓度及时间点)开始给药时间点、给药周期、频率、剂量、给药方式。

注意:科学实验中,动物不可避免地承受着不同程度的疼痛、痛苦甚至死亡,考虑到动物福利与伦理,必须设置适当的人道点。
3. 检测:
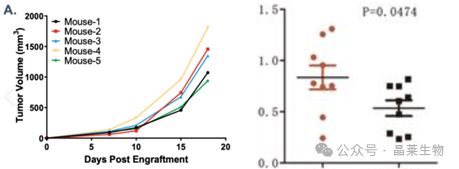
①每2天测量一次瘤子体积
②取材后的瘤子称重
③取材方案目标组织、样本。
④检测:根据项目或课题需求进行对应的检测。
4. 评价标准
① 相对肿瘤增殖率:
相对肿瘤体积RTV= Vt/V0。其中V0为分笼给药时(即d0)测量所得肿瘤体积,Vt为每一次测量时(即dn)的肿瘤体积。
相对肿瘤增殖率T/C(%)=(给药组RTV/对照组RTV)×100%。
T/C(%)>40%为无效;T/C(%)≤40%,并经统计学处理P< 0.05为有效。
②肿瘤生长曲线
除了相对增殖率,不少文献中一般会绘制肿瘤生长曲线,即将肿瘤体积变化对时间作出生长曲线,可由曲线的斜率变化判断药物抑制肿瘤生长的作用。
试验结束后,处死动物,然后剥离瘤块,称瘤重。
肿瘤生长抑制率=(1-治疗组平均瘤重/对照组平均瘤重)×100%。
肿瘤生长抑制率<40%为无效;肿瘤生长抑制率≥40%,并经统计学处理P< 0.05为有效。
注意:出现以下情况,实验结果应判断为无效,需要重复试验:阴性对照组小鼠肿瘤平均瘤重小于1克,或20%小鼠瘤重小于400毫克;大鼠肿瘤平均瘤重小于2克。均表示肿瘤生长不良。
生命延长率是评价抗肿瘤药物的重要标准。
生命延长率=(T/C-1)100%,(T、C分别表示给药组动物存活日数和对照组动物存活日数)。
但是小鼠皮下荷瘤几乎很难死亡,并且考虑到动物福利与伦理学,所以生命延长率并不是理想的观测指标。

关于晶莱
