

药物代谢常被称为生物转化。代谢反应被分为两相:Ⅰ相反应和Ⅱ相反应。代谢稳定性一般被用来描述化合物代谢的速度和程度,是影响药代动力学性质的主要因素之一。代谢和代谢清除率是决定候选化合物整体清除率的主要因素。
肝脏是药物代谢的主要器官,含有大部分代谢活性酶。为获取代谢数据,体外代谢模型如肝微粒体、肝细胞或肝S9经常被选作为体外代谢研究的标准模型。将化合物与酶源(一般选择肝微粒体)孵育后,在不同的时间点采集样品并分析化合物的剩余量,计算半衰期(t1/2)、内在清除率(Cl int)并可预测体内清除率(Clint,in vivo)和肝摄取率(EH)。
药物代谢的重要性:
① 生物利用度的提升:药物在体内的吸收、分布、代谢和排泄过程直接影响其生物利用度。良好的代谢特性可以提高药物的生物利用度,从而减少剂量,降低副作用。
② 减少副作用:通过优化药物代谢,可以减少药物在体内的积累,降低毒性和副作用的风险。
③ 个性化医疗:考虑到个体间代谢差异,药物代谢研究有助于实现个性化医疗,为不同患者提供最适合的药物和剂量。
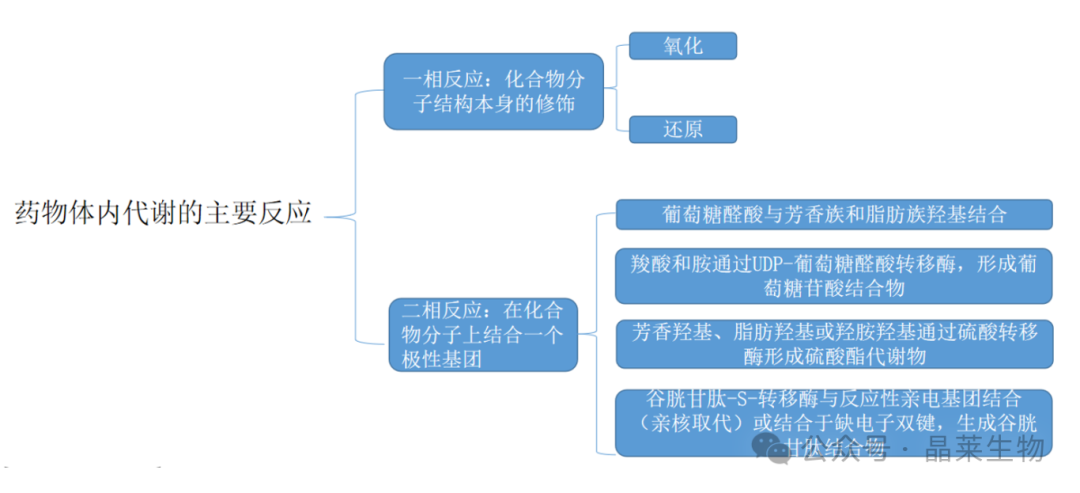
一相代谢通过多种机理修饰化合物结构,包括氧化和还原。
多种不同的酶家族催化这些反应,其中最主要的称为单氧化酶,包括细胞色素P450酶(CYP)家族和黄素单氧化酶(FMO)家族。
单氧化酶的反应通式如下:
R-H+O2+NADPH+H+→R-OH+NADP++H2O
CYP反应受亚铁血红素基团催化,其在活性位点含有一个铁原子。
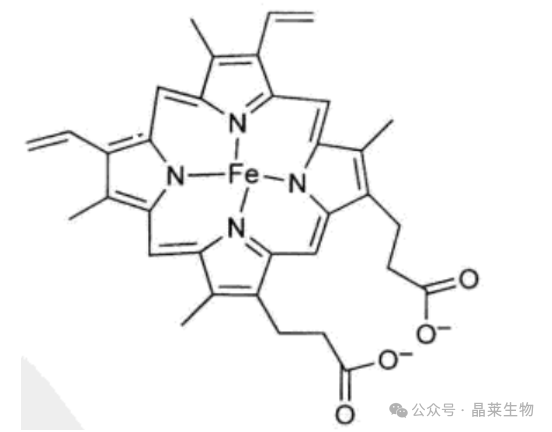
在CYP反应中,铁原子与氧结合,并通过一系列反应将氧转移到药物分子。NADPH通过另一个复合酶(NADPH-细胞色素P450还原酶)为Fe3+还原为Fe2+的反应提供电子。
影响CYP反应速率的因素:
①化合物对CYP酶的亲和力
②化合物分子中可接近亚铁血红素基团位点的反应性
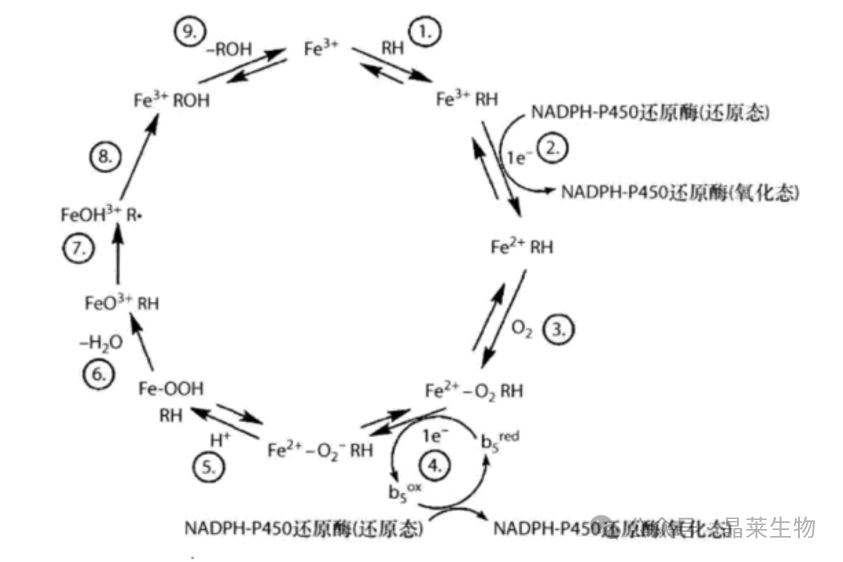
CYP450反应催化循环机理
1. 常见的一相代谢反应
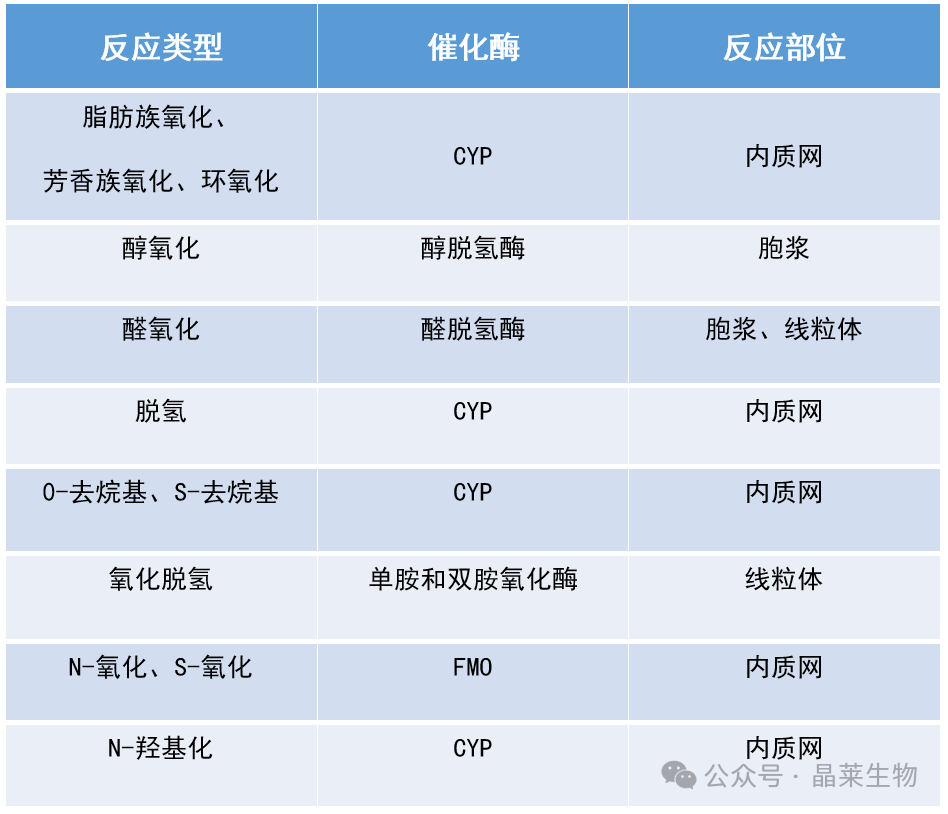
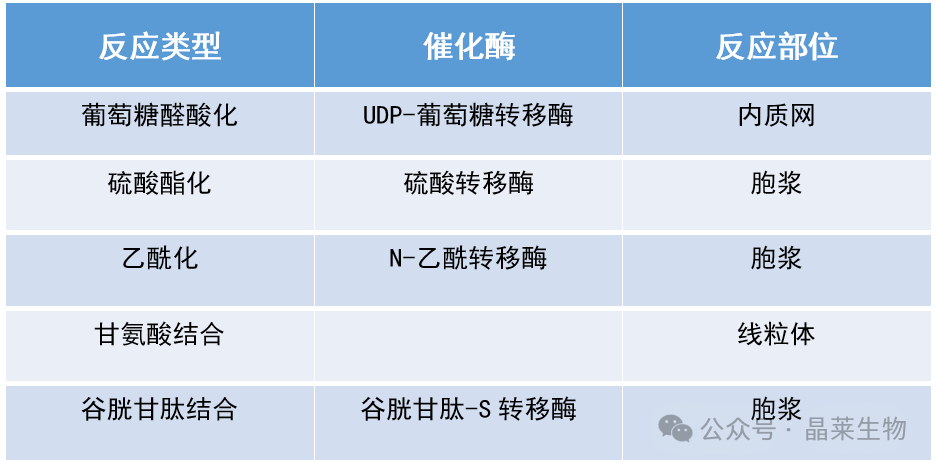
2. 常见二相代谢类型:
二相代谢是在分子中加入极性分子。二相结合物亲水性极大增强,提高药物向胆汁和尿消除。
1. 代谢稳定性对药动学的影响
代谢稳定性与清除率(Cl)呈负相关,代谢稳定性降低导致清除率升高。
Cl和分布容积(Vd)直接影响PK半衰(t1/2=0.693×Vd/Cl),它决定了给药频率。药物清除率和吸收是由肠渗透性和溶解度决定的,直接影响口服生物利用度(F),F决定给药剂量。
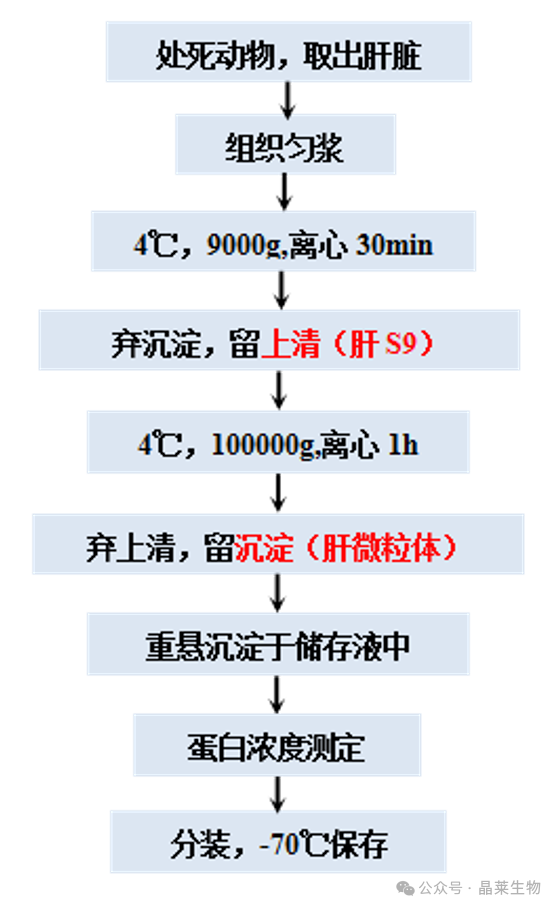
2. 代谢稳定性的研究方法
代谢稳定性是药物发现中化合物最重要的性质之一。稳定性差是先导化合物的主要弱点,需要加以改善。定量的代谢稳定性数据被用于评估代谢的程度,药物化学家可以据此进行结构修饰来改善稳定性。

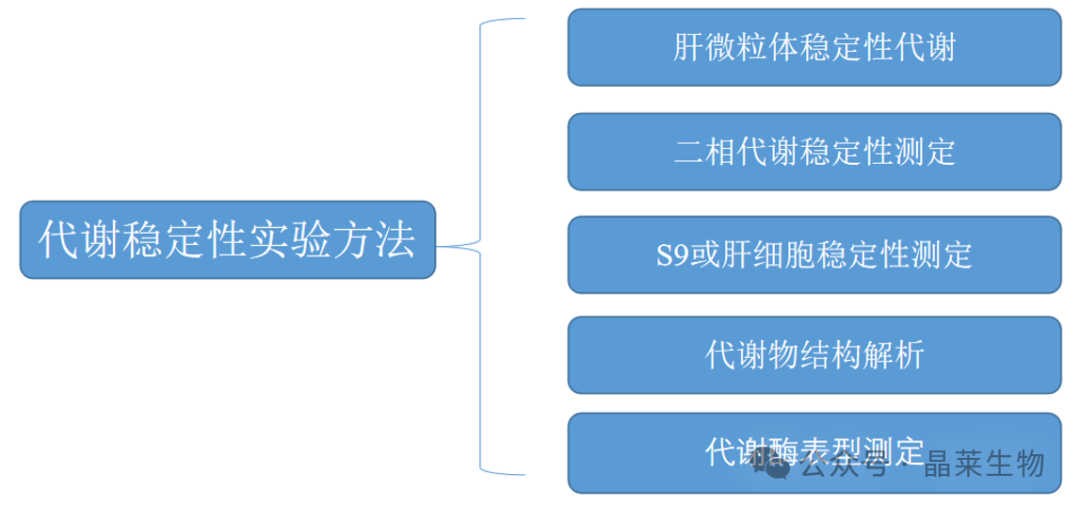
3. 代谢稳定性实验方法
① 分子结构优化:
通过调整药物的化学结构,如引入或去除特定的官能团,可以改变药物在体内的代谢途径和速率。
设计具有更高代谢稳定性的药物分子,以减少其在体内的快速降解,从而延长药物作用时间。
预测和减少有毒代谢产物的生成,通过改变药物结构中的代谢热点或引入代谢屏障基团。
② 前药设计:
前药是药物的无活性或低活性形式,在体内经过酶解或其他化学过程转化为活性药物。
通过设计前药,可以控制药物的释放速率和靶向性,从而减少副作用并提高治疗效果
① 纳米技术应用:
利用纳米技术制备的药物载体,如纳米颗粒、脂质体和聚合物微球,可以显著提高药物的溶解性和生物利用度。
纳米载体还可以保护药物免受体内酶的降解,从而延长药物作用时间。
通过精确控制纳米载体的尺寸和表面性质,可以实现药物的靶向递送。
② 新型辅料和制剂技术:
引入新型辅料,如表面活性剂、稳定剂和增稠剂,以改善药物的溶解度和稳定性。
应用固体分散技术、包合技术和微囊化技术等制剂技术,以提高药物的生物利用度和减少首过效应。
① 药物代谢酶研究:
深入研究药物代谢酶(如CYP450酶系)的底物特异性和抑制剂作用机制,以预测和避免药物间的代谢性相互作用。
通过体外和体内实验,评估药物对代谢酶的诱导或抑制作用,为药物组合使用提供科学依据。
② 药物转运蛋白研究:
研究药物转运蛋白(如P-糖蛋白、MRP等)的底物特异性和调节机制,以预测和避免药物间的转运性相互作用。
通过调整药物结构或制剂形式,以减少对转运蛋白的竞争性抑制或诱导作用。
① 药物代谢相关基因研究:
利用基因组学技术,识别与药物代谢相关的遗传变异(如单核苷酸多态性SNP),以预测个体对药物的代谢速率和反应类型。
通过建立药物代谢基因型数据库和算法模型,为个体化治疗提供科学依据。
② 个体化治疗方案制定:
根据患者的基因组学数据,为患者制定个性化的药物治疗方案,包括药物选择、剂量调整和给药频率等。
通过实时监测患者的药物代谢和疗效指标,及时调整治疗方案,以确保最佳的治疗效果和安全性。

关于晶莱
