

WB 抗体选择的中心逻辑:一抗看“特异性”,二抗看“匹配性”,两者需围绕实验目的、样本类型、检测方法等选择。 一抗选择核心原则及实操 1. 靶点特异性(第一优先级) ① 优先选 WB验证的抗体,厂家说明书明确标注可以做WB。 ② 确认靶点序列:选择针对蛋白特异性区域(避免同源蛋白保守序列)的抗体,如磷酸化抗体需标注“位点特异性”(如 p-AKT Ser473)。 ③ 验证方式:一看厂家提供的 WB 图,选择条带单一、无杂带的;二看引用文献,已经使用验证。 2. 种属反应性匹配 ① 严格匹配样本种属:确认抗体说明书中种属反应性(Reactivity),人源样本选可以做人源靶点的抗体,小鼠样本选小鼠靶点抗体,兔子样本选兔子靶点抗体。 ② 跨种属需确认“交叉反应”。 3. 抗体亚型与形式适配 ① 多见为兔源/鼠源抗体 a. 单克隆抗体:特异性高、杂带少,适合定量 WB 和磷酸化蛋白检测。 b. 多克隆抗体:灵敏度高、结合多表位,适合低丰度蛋白检测。 ② 避免选择仅识别天然构象的抗体(如部分构象表位抗体),WB 样本经 SDS 变性,需选择识别线性表位的抗体。 4. 灵敏度匹配样本丰度 ① 高丰度蛋白(如 GAPDH、β-actin):常规灵敏度抗体即可。 ② 低丰度蛋白(如转录因子、磷酸化蛋白):选高灵敏度抗体(厂家标注“High sensitivity”),或亲和纯化抗体。 ① 优先选较稳定的品牌:如CST、Abcam,避免无验证数据的小众抗体。 ② 磷酸化抗体额外注意:必须选“位点特异性”,且蛋白提取过程需要加磷酸酶抑制剂,避免脱磷酸化导致无条带。 ③ 稀释比例参考:以厂家推荐稀释为主,例如1:500-1:2000,可以选择1:1000,低丰度蛋白可降升高浓度至 1:500,高丰度可降低浓度至1:2000,有条件可以通过预实验优化。 ④ 对照设置:设置阳性对照(已知表达靶点的样本)、阴性对照(敲除 / 敲低靶点的样本),排除非特异条带。 二抗选择核心原则及实操 1. 严格匹配一抗种属 + 亚型 二抗需针对一抗的种属和 IgG 亚型: 一抗为兔源(Rabbit IgG)→选山羊抗兔 IgG 二抗(Goat anti-Rabbit IgG); 一抗为鼠源(Mouse IgG)→选山羊抗鼠 IgG 二抗(Goat anti-Mouse IgG); 若一抗为其他种属(如山羊、大鼠),需对应匹配(如兔抗山羊 IgG)。 避免种属 / 亚型错配,否则无信号或非特异结合。 2. 标记类型适配检测方法 ① 常规化学发光 WB(ECL):选HRP 标记二抗(辣根过氧化物酶),性价比高、灵敏度适中; ② 荧光 WB(近红外检测):选荧光标记二抗(如 Alexa Fluor 680/790、IRDye 800CW),适合双色定量和低背景检测; ③ 避免标记类型错配(如荧光二抗用于 ECL 检测无信号)。 3. 特异性降低背景干扰 ① 优先选亲和纯化二抗,或标注“Minimal cross-reactivity”(最小交叉反应)的二抗,减少与样本内源性蛋白的结合。 ② 若样本含血清(如细胞上清),选预吸附二抗(吸附过样本种属血清蛋白),避免血清 IgG 干扰。 ③ 适当降低二抗浓度降低背景。 4. 灵敏度匹配实验需求 ① 低丰度蛋白:选高灵敏度 HRP 二抗(如增强型 HRP)或荧光二抗(信号更稳定); ② 高背景样本:选特异性更高的单克隆二抗,或降低二抗浓度。 总结 一抗:WB 验证 + 种属匹配 + 特异性优先,低丰度选高灵敏度,磷酸化选位点特异性; 二抗:严格匹配一抗种属/亚型,HRP适配常规WB; 实操:以厂家推荐为基础,通过预实验优化稀释比,必要时设置对照排除干扰。 关于晶莱


5. 实操选择技巧
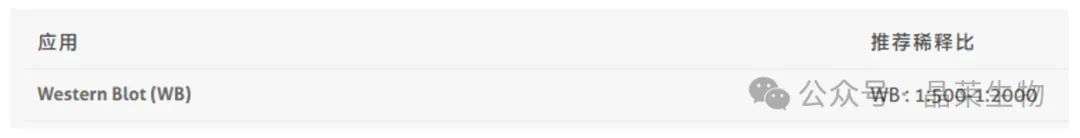
5. 实操选择技巧
① 二抗来源选择:优先选山羊源二抗,性价比高;若需多色检测,选不同荧光标记的同一种属二抗。
② 稀释比例优化:HRP 二抗常规 1:5000-1:10000看厂家推荐稀释比例,根据背景和信号强度调整(背景高则降低浓度,信号弱则升高)。
③ 封闭液匹配:二抗为山羊源时,封闭液选5% 脱脂牛奶(常规)或BSA(磷酸化抗体专用,避免牛奶中磷酸化蛋白干扰);避免封闭液与二抗种属冲突(如兔源二抗不用兔血清封闭)。
④ 二抗对照:设“仅二抗对照”(不加一抗,其余步骤相同),若有条带则为二抗非特异结合,需更换二抗或优化封闭 / 洗涤。
