

急性肝损伤(Acute liver injury,ALI)是急性肝衰竭的基础,严重或持续的肝损伤,最终导致急性重症肝炎或爆发性肝炎而死亡。目前建立急性肝损伤模型的方法主要有病毒性模型、免疫性模型及化学性模型,其中化学性模型又以四氯化碳和内毒素致动物急性肝损伤模型较为常用。研究表明,内毒素不仅可以直接或间接造成肝细胞的损伤,而且其诱导的肝细胞坏死在重 症肝炎的发展进程中起重要作用。脂多糖(LPS)是内毒素的主要毒性作用成分,可介导炎症因子破坏血管内皮的完整性,导致肝凋亡和坏死, 同时引起肝脏的损伤及出血。D-氨基半乳糖(D-Gal)是常用的化学性肝毒性药物,可快速结合并消耗大量的尿苷酸,影响肝细胞蛋白质、酶等的生成,从而对肝细胞组织造成不可逆的损伤。利用LPS/Gal诱导动物发生急性肝损伤,不仅能建立内毒素性急性肝损伤动物模型,同时可用于急性重症肝炎模型的研究。
一、常用急性肝损伤动物模型造模方法
1. 药物诱导模型
对乙酰氨基酚(APAP)模型
机制:APAP经CYP450(CYP2E1/CYP3A4)代谢为毒性产物NAPQI,耗竭谷胱甘肽(GSH),引发线粒体氧化应激和坏死性凋亡。
关键蛋白:CYP2E1(代谢激活)、Nrf2(抗氧化应答)、JNK(应激信号放大)、MLKL(坏死性凋亡执行蛋白)。
临床关联:APAP是药物性肝损伤(DILI)最常见病因,临床治疗依赖N-乙酰半胱氨酸(NAC)补充GSH。
四氯化碳(CCl₄)模型
机制:CCl₄经CYP2E1代谢生成三氯甲基自由基(·CCl₃),引发脂质过氧化和肝细胞膜破坏,激活星状细胞导致纤维化。
关键蛋白:TNF-α(炎症放大)、TGF-β1(促纤维化)、Collagen I(纤维化标志物)。
临床关联:用于研究肝纤维化向肝硬化转化的机制,抗纤维化药物(如吡非尼酮)的临床前验证。
2. 酒精性肝损伤模型
慢性乙醇灌胃/液体饲料模型
机制:乙醇经ADH/CYP2E1代谢生成乙醛和ROS,诱导肠道菌群紊乱(LPS入血激活TLR4通路)和脂肪变性。
关键蛋白:TLR4/NF-κB(炎症)、SREBP-1c(脂肪合成)、CYP2E1(氧化应激)。
临床关联:研究酒精性肝炎(AH)的炎症靶点,临床试验探索抗TLR4抗体(如JKB-121)的疗效。
3. 缺血再灌注(I/R)损伤模型
部分肝缺血或原位肝血流阻断
机制:缺血期缺氧导致ATP耗竭,再灌注期ROS爆发激活Kupffer细胞释放促炎因子(如IL-1β、TNF-α)。
关键蛋白:HIF-1α(缺氧应答)、补体C3/C5a(炎症放大)、NLRP3炎性小体。
临床关联:肝移植和肝切除手术中I/R损伤的防治,临床试用ROS清除剂(如依达拉奉)。
4. 免疫介导模型
刀豆蛋白A(ConA)模型
机制:ConA激活T细胞和巨噬细胞,通过Fas/FasL通路诱导肝细胞凋亡,模拟自身免疫性肝炎。
关键蛋白:Fas/FasL(凋亡信号)、IFN-γ(Th1免疫应答)、Granzyme B(细胞毒性)。
临床关联:探索免疫抑制剂(如糖皮质激素)或抗FasL抗体(如APG101)的疗效。
5. 胆汁淤积性模型
胆总管结扎(BDL)模型
机制:胆酸蓄积激活FXR受体,诱导肝细胞凋亡和胆管反应性增生。
关键蛋白:FXR(胆酸调控)、Caspase-3(凋亡)、CK19(胆管标志物)。
临床关联:研究原发性胆汁性胆管炎(PBC),熊去氧胆酸(UDCA)的临床验证。
二、核心机制通路与靶点
1. 氧化应激通路
关键分子:NADPH氧化酶(NOX)、Nrf2-Keap1通路。
干预靶点:NAC、褪黑素、SIRT1激活剂(如白藜芦醇)。
2. 炎症信号通路
TLR4/MyD88/NF-κB通路:介导LPS诱导的炎症级联反应。
NLRP3炎性小体:驱动IL-1β成熟释放。
3. 细胞死亡通路
坏死性凋亡(Necroptosis):RIPK1-RIPK3-MLKL轴。
凋亡(Apoptosis):线粒体途径(Bax/Bak→Caspase-9→Caspase-3)。
4. 代谢紊乱通路
脂质代谢:SREBP-1c/PPARα失衡导致脂肪蓄积。
胆酸毒性:FXR/SHP调控胆酸合成。
三、临床转化研究进展
抗氧化治疗:NAC用于APAP中毒(临床一线),但需早期给药。
抗炎靶向药:抗TNF-α单抗(如英夫利昔)在酒精性肝炎中因感染风险受限。
细胞死亡抑制剂:Necrostatin-1(RIPK1抑制剂)处于临床前阶段。
肠道-肝脏轴干预:益生菌(如VSL#3)调节肠道菌群,减少LPS入血。
基因治疗:腺病毒载体递送IL-10或siRNA沉默TGF-β1(动物模型有效)。
四、模型选择与局限性
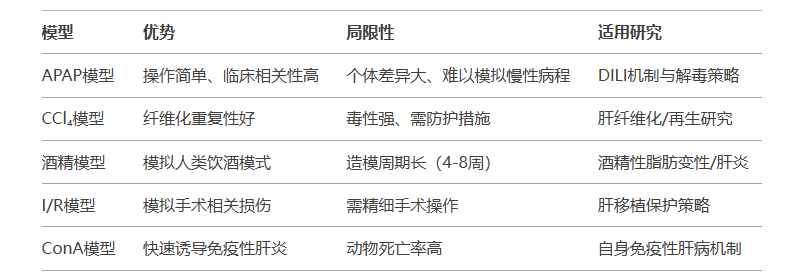
五、未来研究方向
多模型联合应用:如APAP叠加酒精模型模拟多重打击机制。
类器官与芯片肝脏:减少动物实验,提高人源化研究比例。
精准靶向治疗:基于单细胞测序筛选亚群特异性靶点。
生物标志物开发:如miR-122、HMGB1用于早期诊断。
急性肝损伤动物模型的机制研究已揭示氧化应激、炎症、细胞死亡等核心通路,关键蛋白(如CYP2E1、TLR4、MLKL)为临床干预提供了靶点。未来需结合多组学技术和临床队列验证,加速转化医学进程。
晶莱生物服务流程
晶莱生物实验服务项目
| 动物实验 | 细胞生物学 | 病理实验 |
| 消化系统模型 | 细胞培养 | 病理染色 |
| 胃酸分泌模型 | 普通细胞株 | HE染色 |
| 脓毒症模型 | 细胞缺氧培养 | 油红O染色 |
| 胃溃疡模型 | 细胞培养+支架 | 番红固绿染色 |
| 胰腺炎模型 | 干细胞培养 | Masson染色 |
| 肝纤维化模型 | 原代细胞分离/提取/培养 | 天狼猩红染色 |
| DIO肥胖模型 | 细胞转染/病毒感染 | PAS糖原染色 |
| 胆结石模型 | Trans well共培养 | 阿利新蓝染色 |
| 结肠炎(UC)模型 | 细胞增殖 | 甲苯胺蓝染色 |
| 脂肪肝模型 | 细胞计数 | 尼氏染色 |
| 急性肝损伤模型 | 生长曲线测定 | LFB髓鞘染色 |
| 免疫、代谢系统疾病模型 | 存活曲线测定 | 普鲁士蓝染色 |
| 骨质疏松模型 | ccK-8增殖检测 | VG染色 |
| 糖尿病模型 | MTT增殖检测 | EVG染色 |
| 高尿酸血症模型 | CFSE检测增殖-流式检测 | VonKossa染色 |
| 呼吸系统模型 | BrDU检测-免疫荧光法 | 刚果红染色 |
| 肺纤维化模型 | 细胞凋亡 | 苏丹黑B染色 |
| 慢性肺阻塞模型 | Annexin V/PI流式检测细胞凋亡 | Trap染色 |
| 急性肺损伤模型 | WB检测凋亡相关蛋白 | 抗酸染色 |
| 哮喘模型 | 透射电镜观察凋亡小体 | 革兰氏染色 |
| 肺栓塞模型 | Tunel染色(POD法,DAB显色) | AB-PAS染色 |
| 支气管炎模型 | Tunel(荧光法,含试剂盒) | 亚甲基蓝染色 |
| 泌尿生殖系统模型 | DNA ladder法 | 苯胺蓝染色 |
| 慢性肾衰模型 | 细胞周期 | 荧光 DAPI染色 |
| 急性肾衰模型 | 细胞显微计数 | 普鲁士蓝染色 |
| 肾间质纤维化模型 | PI染色 | 间苯二酚碱性品红染色 |
| 肾结石模型 | BrdU渗入法 | 银染 |
| 肾炎模型 | 免疫荧光染色 | 黑色素染色 |
| 子宫内膜异位症模型 | PI流式检测细胞周期 | 镀银染色 |
| 心血管系统模型 | 细胞运动 | PASM 六胺银染色 |
| 冠心病模型 | Transwell检测细胞迁移 | VG染色 |
| 心肌梗死模型 | Transwell检测细胞侵袭 | 富尔根染色 |
| 心脏骤停模型 | 细胞划痕 | 亚甲基蓝染色 |
| 慢性心力衰竭模型 | 细胞克隆 | 碘-碘化钾染色 |
| 动脉粥样硬化模型 | 集落形成法/稀释铺板方法 | Goldner三色法染色 |
| 白血病模型 | 软琼脂克隆法 | PAS-萘酚磺S染色 |
| 高血压模型 | 毛细管克隆法 | 改良苯酚品红染色 |
| 神经系统模型 | 体外实验血管生成 | 网状纤维染色 |
| 脑卒中模型 | 磁珠分选细胞 | β-半乳糖苷酶染色 |
| 栓塞性脑梗死模型 | 流式分选细胞 | 镀银染色 |
| 脑出血模型 | 开机费 | movat五色染色 |
| 脑损伤模型 | 单色 | 维多利亚蓝染色 |
| 脊髓损伤模型 | 双色 | 免疫组化 |
| 帕金森模型 | CBA多细胞因子流式检测 | 免疫组化预式 |
| 老年痴呆模型 | 组织/血液细胞制备 | 免疫组化正式 |
| 应激模型 | 组织单细胞制备 | 免疫荧光(石蜡-单标) |
| 骨骼疾病模型 | 中性粒细胞提取 | 免疫荧光(石蜡-双标) |
| 骨折模型 | 其他样本细胞制备(如血液等) | 免疫荧光(石蜡-三标) |
| 骨缺损模型 | 外周血PBMC分离 | 免疫荧光(冰冻-单标) |
| 风湿免疫性关节炎模型 | 线粒体组学 | 免疫荧光(冰冻-双标) |
| 骨关节炎模型 | 线粒体膜电位检测-流式法 | 制片前处理 |
| 五官疾病模型 | 线粒体膜电位检测-免疫荧光法 | 石蜡组织包埋 |
| 眼科疾病模型 | 线粒体ROS生物含量检测--流式 | 特殊包埋(细胞、材料、眼球等) |
| 鼻腔疾病模型 | 线粒体ROS生物含量检测--免疫荧光 | 软化(肝硬化、皮肤结痂、植物等) |
| 皮肤疾病模型 | 线粒体通透性转换孔(mPTP) | 骨组织脱钙(小) |
| 皮肤损伤模型 | 溶酶体免疫荧光法 | 骨组织脱钙(大) |
| 肿瘤疾病模型 | 线粒体+溶酶体共定位 | 骨组织EDTA脱钙(小) |
| 原位瘤模型 | 内质网 | 骨组织EDTA脱钙(大) |
| 转移瘤模型 | 线粒体钙瞬时变化检测-流式 | 石蜡白片 |
| 皮下植瘤模型 | ATP检测 | 细胞爬片 |
| ADP检测 | ||
| AMP检测 | ||
| 流式 | DNA/RNA半定量检测 | 基因编辑工具 |
| 组织细胞悬液处理 | pcr检测mRNA | 合成(3保1)片段/质粒/引物合成 |
| 细胞处理 | microRNA检测 | 质粒载体构建 |
| 血液标本处理 | LncRNA表达量的检测 | 过表达腺病毒载体构建包装 |
| 细胞刺激培养 | CirRNA表达量的检测 | shRNA腺病毒载体构建包装 |
| 单色检测 | 凝胶电泳 | 过表达慢病毒载体构建包装 |
| 双色检测 | 基因合成 | shRNA慢病毒载体构建包装 |
| Annexin V/PI凋亡 | <300 | 过表达腺相关病毒载体构建包装 |
| 细胞周期 | 300-1,500 | shRNA腺病毒载体构建包装 |
| 1500 - 5000 | 稳转细胞株 | |
| >5000 | ||
| 特殊序列 | ||
| ELISA | WB | qPCR |
| 组织匀浆处理 | 蛋白提取及定量一 | RNA抽提 |
| ELISA(不含试剂盒)48T/kit | WB检测一(10孔膜/指标) | mRNA引物设计及合成 |
| ELISA(不含试剂盒)96T/kit | 灰度值分析及作图一(10孔膜/指标) | miRNA引物设计及合成 |
| ELISA(含国产试剂盒)48T/kit | 蛋白提取及定量二 | LncRNA引物设计及合成 |
| ELISA(含国产试剂盒)96T/kit | WB检测二(15孔膜/指标) | CircRNA引物设计及合成 |
| 灰度值分析及作图二(15孔膜/指标) | mRNA RT-qPCR | |
| miRNA RT-qPCR | ||
| LncRNA RT-qPCR | ||
| CircRNA RT-qPCR |
收费标准/服务周期/提供结果:
欢迎咨询详谈,我们会根据您的方案及需求制定详细的服务协议。
更多实验技术服务请浏览网站其他内容,或来电咨询!
做实验,找晶莱!您的科研生涯,我们一路相伴!
【平台项目开展范围】慢病毒,腺病毒,RNAi类,分子生物实验,病理实验,免疫学实验,细胞实验,动物实验,蛋白组学实验,芯片类实验,并为广大客户朋友们提供课题设计指导、基金申请指导等服务。