


文献研究目标包括:
1.通过经典标志物(HT-II-280、前表面活性蛋白 C、板层小体)评估传代中关键 AT-II 相关特征的保留情况;
2.评估冻存可行性与类器官生物样本库构建潜力;
3.通过细胞外通量分析比较健康与纤维化 AT-II 类器官的代谢差异。我们假设纤维化 AT-II 细胞相较对照呈现更强糖酵解代谢,反映疾病相关代谢重编程。本研究通过提供明确、可转移的实验方案,建立可重复的人 AT-II 类器官培养框架,支持间质性肺病上皮功能障碍机制研究。
1.研究背景与意义
① 特发性肺纤维化(IPF)是致死性间质性肺病,预后差、无根治手段,急需能模拟人肺病变的体外模型。
② AT‑Ⅱ细胞是肺泡修复的关键干细胞,在纤维化中出现凋亡、衰老、异常分化及代谢重编程(向有氧糖酵解转换)。
③传统2D培养会快速导致AT‑Ⅱ去分化,现有类器官模型多依赖小鼠或iPSC,难以反映终末期患者原代细胞的真实表型与代谢特征。
2. 科学问题:能否建立稳定、可扩增、可冻存的人原代AT‑Ⅱ细胞3D类器官,并在该模型上重现纤维化相关的表型与代谢改变?
3.研究假设:纤维化来源的AT‑Ⅱ类器官会呈现更强的糖酵解代谢(Warburg样表型),反映疾病相关的能量重编程。
4.研究目标
①优化培养条件,稳定维持AT‑Ⅱ表型并抑制异常分化。
②验证冻存可行性,支持生物样本库。
③对比健康/纤维化类器官的代谢差异,验证疾病表型。
1:高纯度分离AT‑Ⅱ与AT‑Ⅰ细胞
核心结果:用HT‑II‑280磁珠分选从63例人肺组织成功分离出高纯度AT‑Ⅱ细胞(纯度≈84%双阳性),AT‑Ⅰ细胞纯度≈93%。

基于分选的分离流程示意图
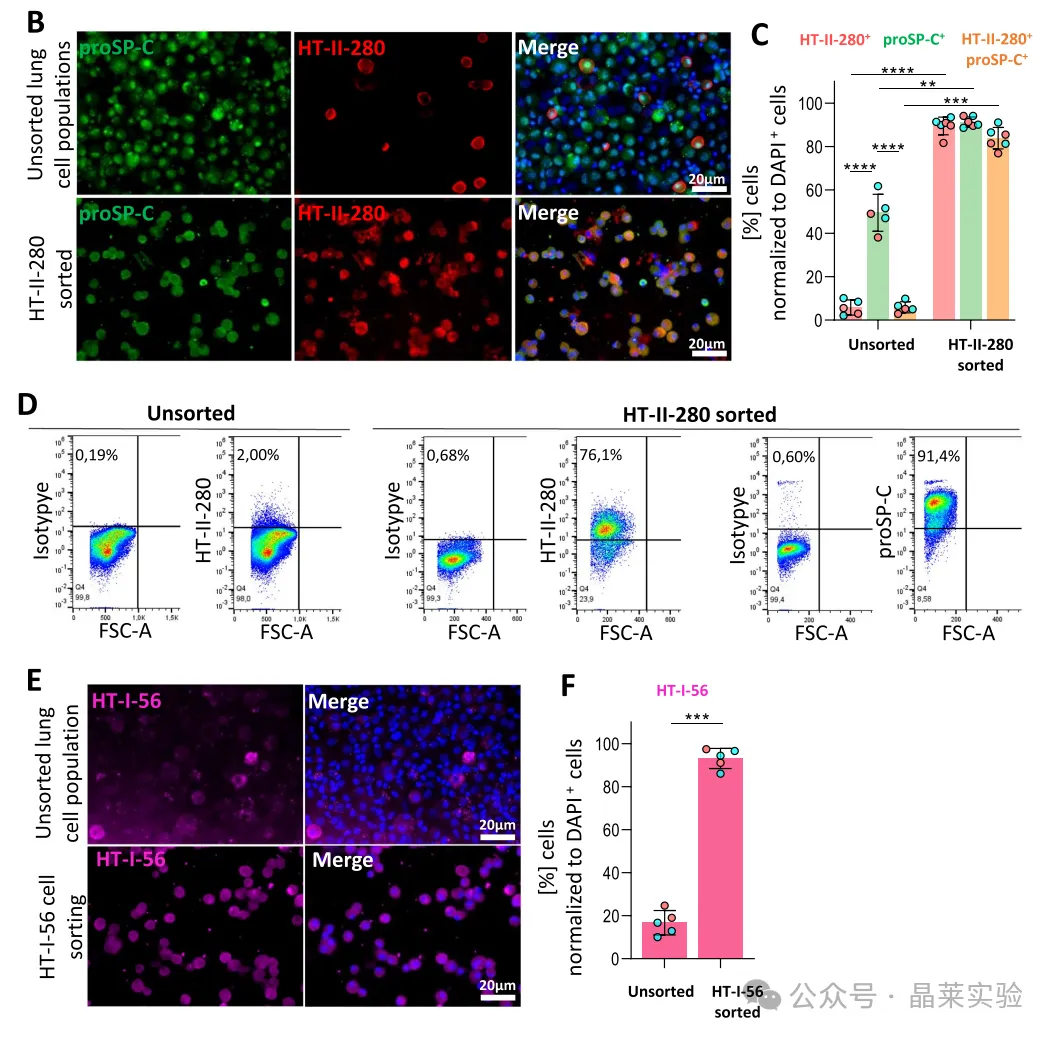
B/C:分选后HT‑II‑280⁺/proSP‑C⁺双阳性细胞显著富集,远高于未分选组。
D:流式证实分选后HT‑II‑280强阳性。
E/F:同步可高纯度分离AT‑Ⅰ细胞(HT‑I‑56⁺)。
关键意义:为后续类器官提供了高纯度、高活力的起始细胞。
2:3D培养条件优化
核心结果:原1:1培养基/Matrigel比例会导致dome塌陷、细胞接触塑料而去分化为基底样细胞(KRT17⁺/CTSE⁺,丢失HT‑II‑280)。
优化为5:8培养基:Matrigel后,dome稳定,避免机械应力诱导的异常分化。
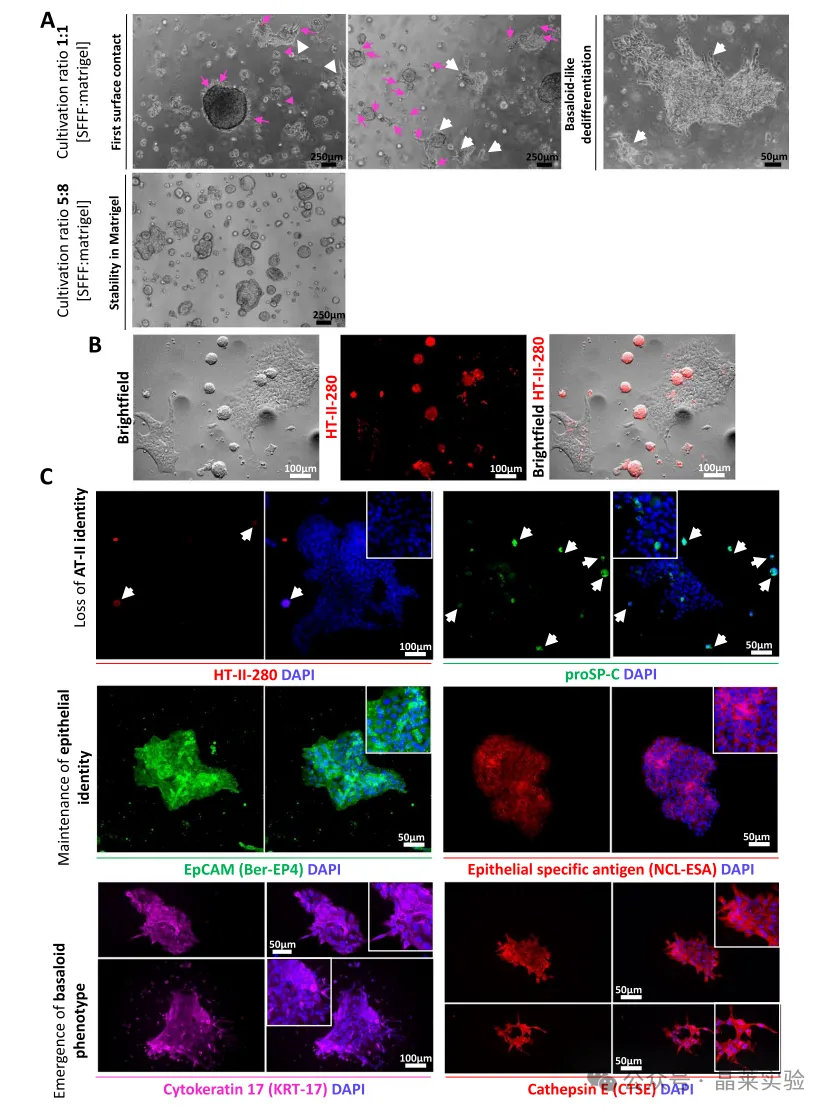
A:1:1比例出现细胞脱落、铺展、基底样转化;5:8比例保持正常肺泡球体形态。
B/C:基底样细胞丢失AT‑Ⅱ标志,但保留上皮标志并表达基底标志物。
关键意义:解决了原代AT‑Ⅱ体外易去分化的核心技术难题。
3:类器官形态与生长能力
核心结果:AT‑Ⅱ细胞高效形成肺泡球体(alveolospheres),形态多样(单囊/多囊/致密无腔),大小50–600μm。纤维化来源类器官集落形成率(CFR)显著更高,P0即达65.4%,健康组仅41.5%;P1均>90%。
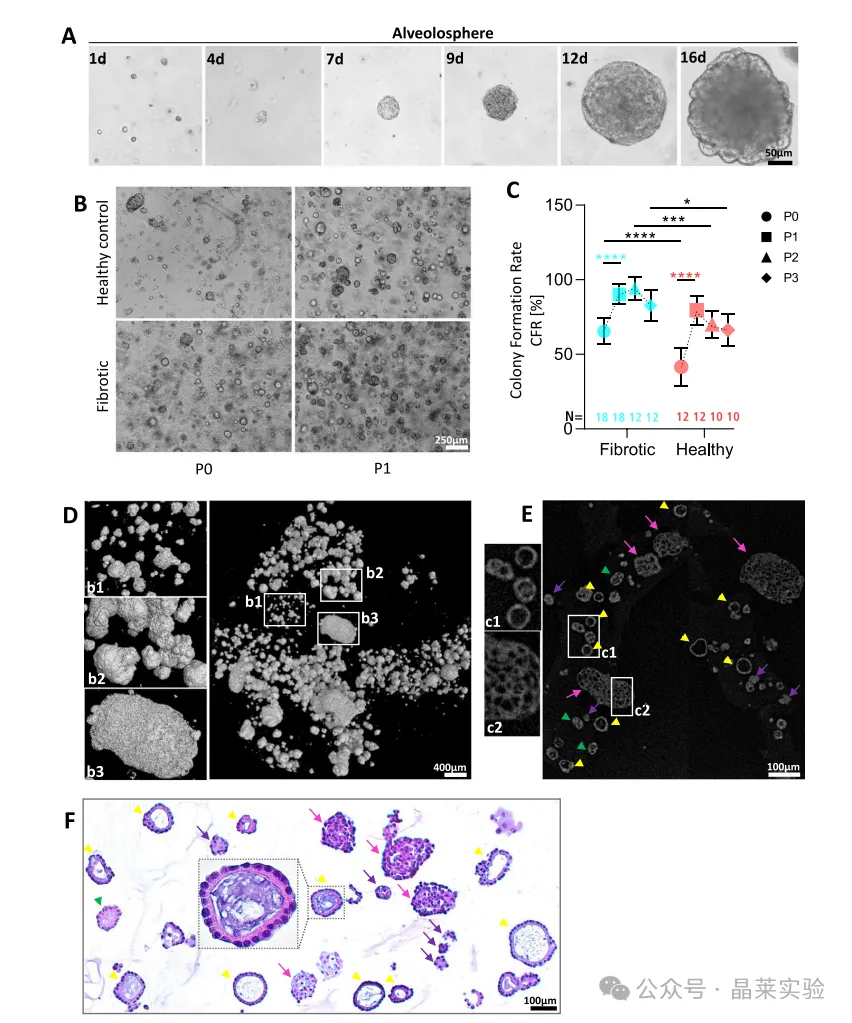
A/B:14天内形成典型肺泡球体,可稳定传代至P3。
C:CFR在P0–P1显著上升,纤维化组全程高于健康组。
D–F:显微CT与H&E显示形态异质性,符合人肺泡结构特征。
关键意义:证明体系可稳定扩增,且纤维化细胞具有更强增殖能力。
4:AT‑Ⅱ表型稳定维持
核心结果:类器官持续表达AT‑Ⅱ关键标志:proSP‑C全程稳定(≈80%–90%阳性),HT‑II‑280略有下降但仍高表达。仅极少量向AT‑Ⅰ分化(HT‑I‑56⁺细胞<15%,P3)。超微结构见大量板层小体,证实成熟AT‑Ⅱ功能。
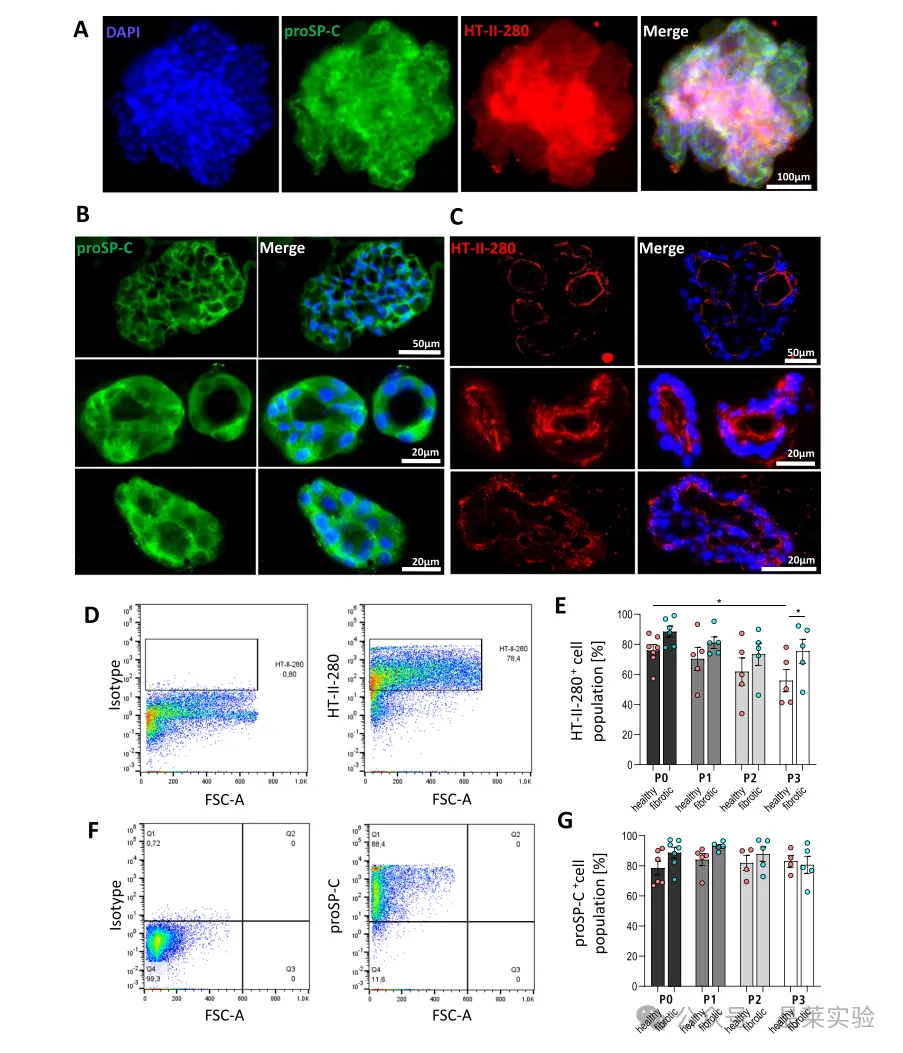
A–G:免疫荧光与流式证实proSP‑C稳定、HT‑II‑280轻度下降。
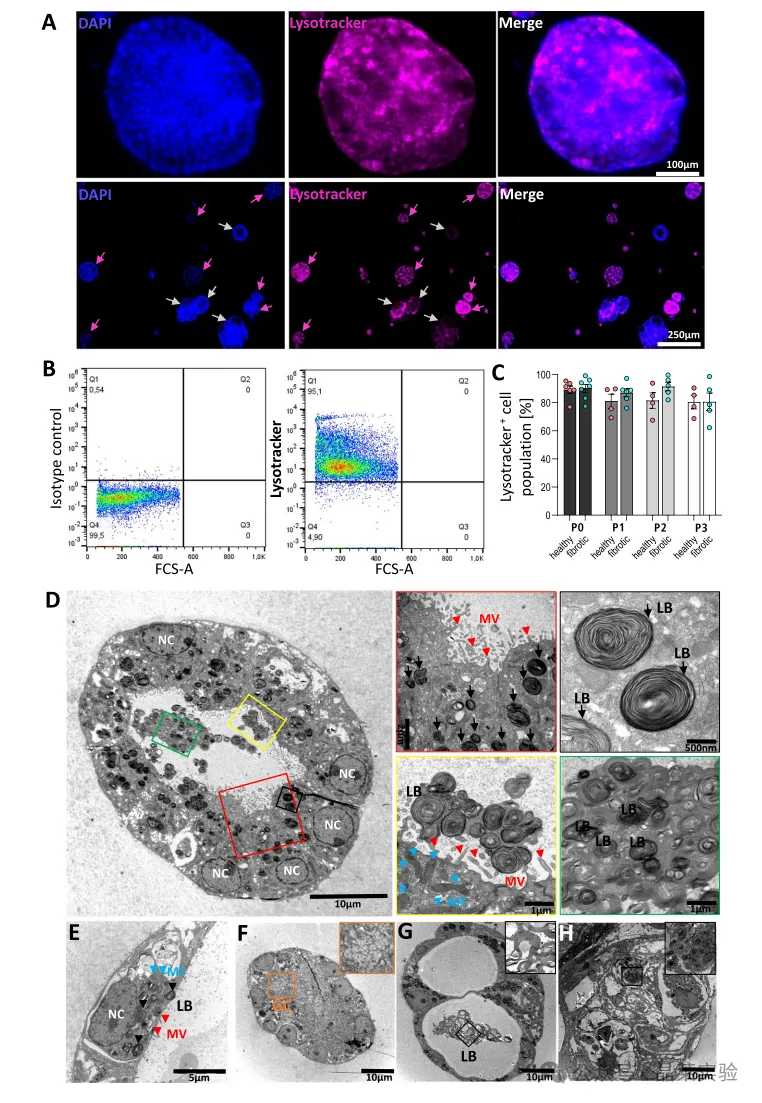
A–H:Lysotracker与TEM证实板层小体存在,为AT‑Ⅱ标志性结构。
关键意义:证明体系能长期维持AT‑Ⅱ干性与功能表型,不发生异常分化。
5:冻存后仍保持高活力与功能
核心结果:类器官经-150℃冻存≥28天,复苏后活力、集落形成、代谢活性无明显下降。凋亡与细胞毒性仅健康组轻微上升,纤维化组无显著变化。
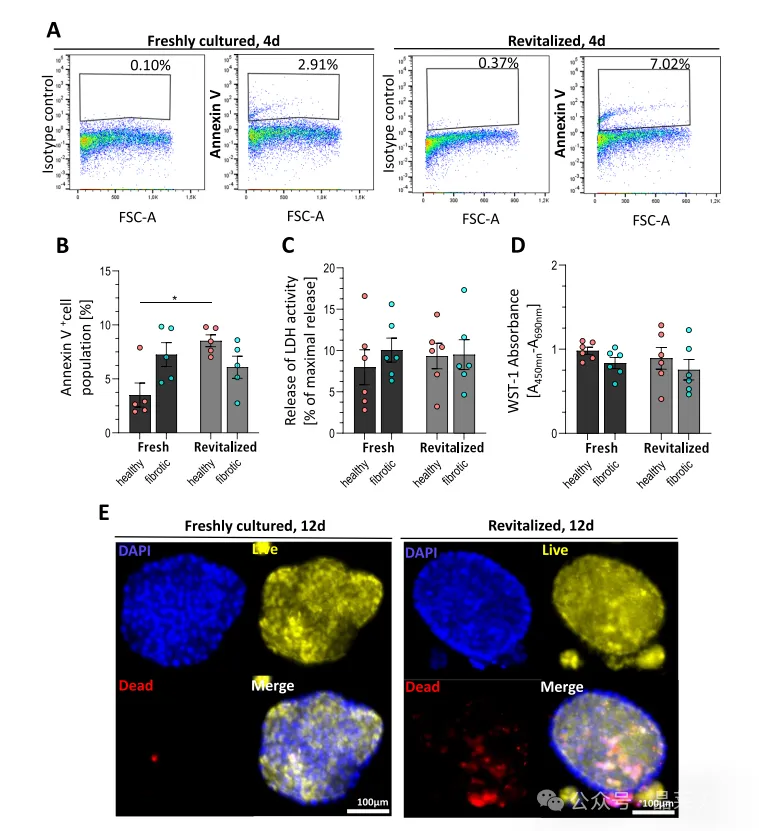
A–E:AnnexinV、LDH、WST‑1、活死染色均证实冻存安全可靠。
关键意义:支持样本库建设与多中心复用,大幅提升实用性。
6:纤维化类器官呈现典型糖酵解重编程
核心结果(最关键发现):
①IPF类器官基础糖酵解升高3倍,代偿性糖酵解升高3.5倍。
②ATP产量提升2.2倍,且主要来自糖酵解(IPF:77.9%;健康:42.9%)。
③氧化磷酸化无明显变化,呈典型Warburg样表型。
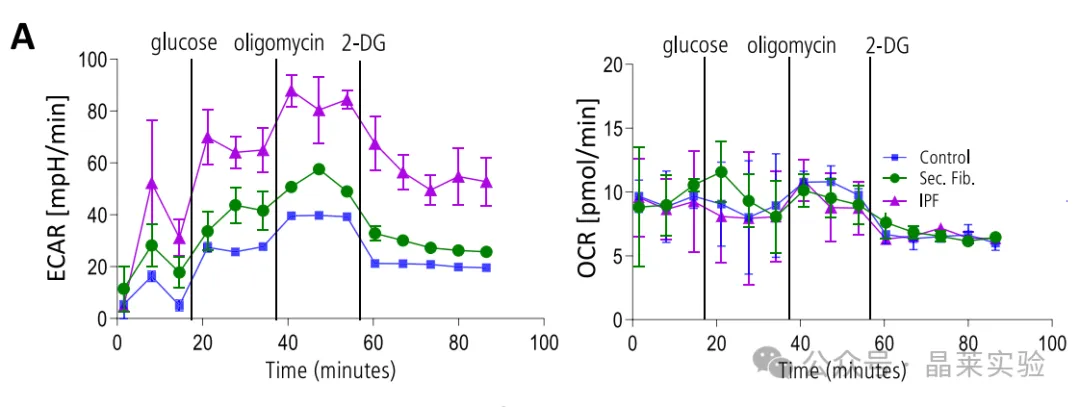
A.代表性代谢检测曲线
对培养12天的原代AT‑Ⅱ细胞(分别来自特发性肺纤维化、继发性纤维化或健康组织)进行细胞外酸化率(ECAR)及对应耗氧率(OCR)的代表性检测。本部分数据共纳入18例患者(7例癌旁对照组织、6例继发性纤维化组织、5例特发性肺纤维化组织),结果显示:特发性肺纤维化(IPF)来源的AT‑Ⅱ类器官基础糖酵解速率呈升高趋势(B),且代偿性糖酵解速率存在显著差异(C)。
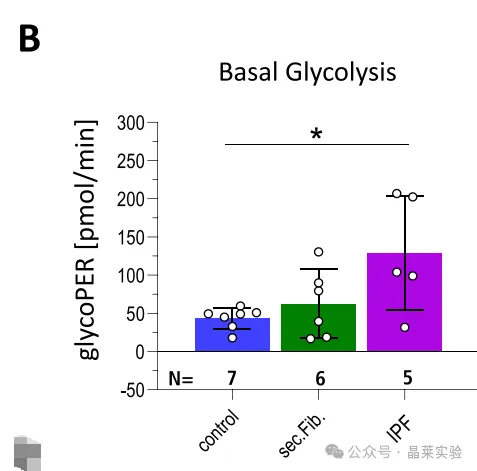
B.基础糖酵解定量统计
采用单因素方差分析(F=4.954;*P=0.0233),后续行Tukey多重比较检验。组间差异:
对照组vs.特发性肺纤维化组:*P=0.0201(显著升高)
对照组vs.继发性纤维化组:P=0.7577(无统计学差异)
继发性纤维化组vs.特发性肺纤维化组:P=0.0852(无统计学差异)
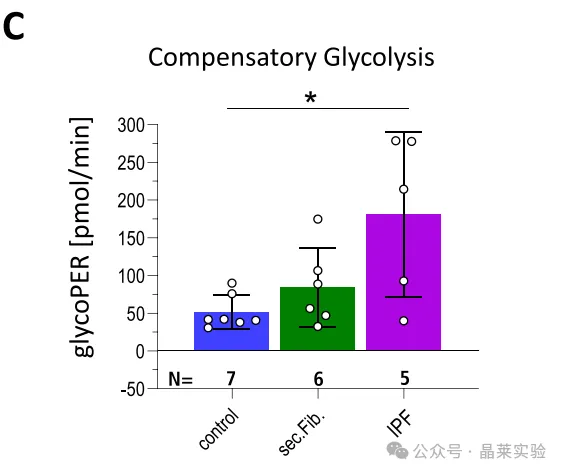
C.代偿性糖酵解定量统计
采用单因素方差分析(F=5.905;*P=0.0128),后续行Tukey多重比较检验。组间差异:
对照组vs.特发性肺纤维化组:*P=0.0109(显著升高)
对照组vs.继发性纤维化组:P=0.6455(无统计学差异)
继发性纤维化组vs.特发性肺纤维化组:P=0.0679(无统计学差异)
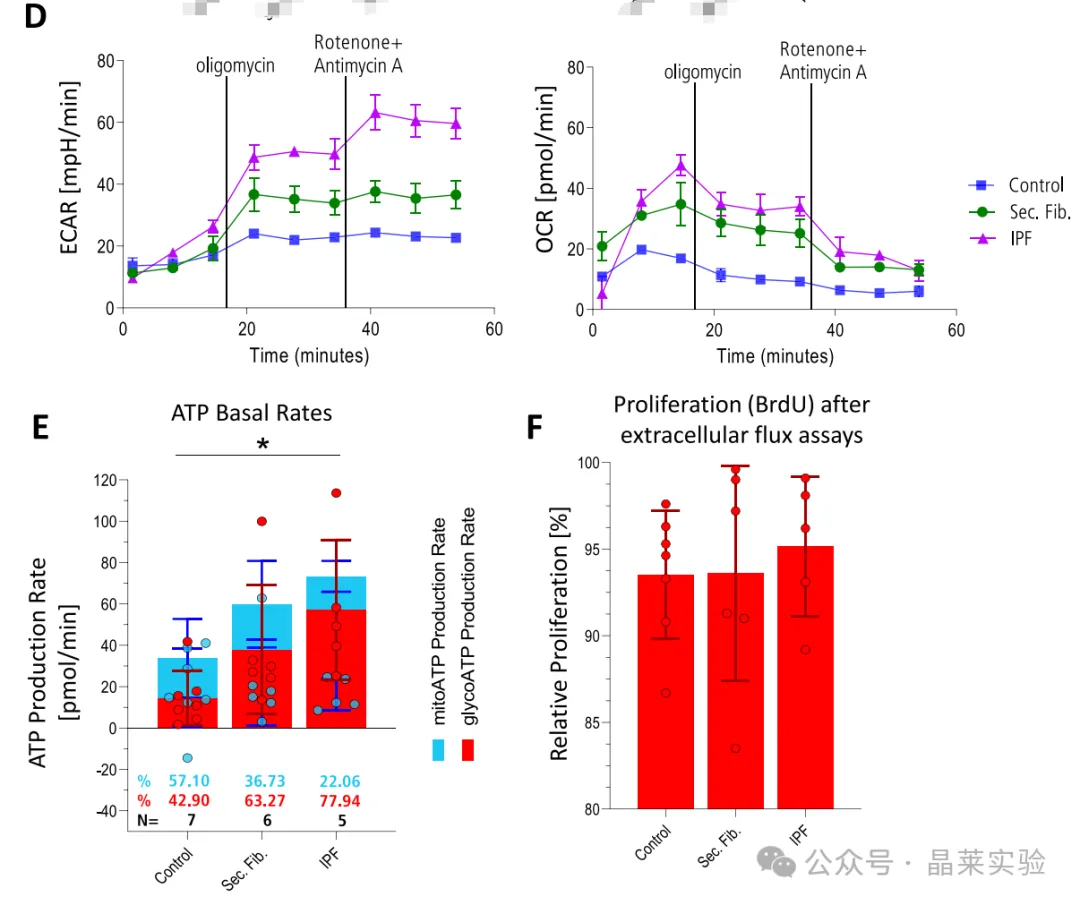
D-E.ATP生成速率检测
为评估ATP生成速率,先向检测培养基中加入寡霉素,再加入鱼藤酮+抗霉素A(RotAA)进行检测。基于代表性ECAR与OCR数据(D),结合**总糖酵解ATP(glyoATP)与线粒体ATP(mitoATP)**生成量,计算总ATP生成速率(E)。图E展示了上述18例患者样本中,基础总ATP生成速率中糖酵解ATP与线粒体ATP的占比分布。
ATP生成量评估采用单因素方差分析(F=3.881;*P=0.401),后续行Tukey多重比较检验。组间差异:
对照组vs.特发性肺纤维化组:*P=0.0477(显著升高)
对照组vs.继发性纤维化组:P=0.1228(无统计学差异)
继发性纤维化组vs.特发性肺纤维化组:P=0.4473(无统计学差异)
F.细胞增殖活性验证
BrdU检测结果显示,细胞外通量实验后,类器官内AT‑Ⅱ细胞的增殖活性未出现显著下降。图中展示相对增殖率(%),计算公式为:(细胞外通量实验后450nm吸光度值/细胞外通量实验前450nm吸光度值)×100%。
关键意义:首次在人原代纤维化AT‑Ⅱ类器官中稳定重现疾病特异性代谢表型,可用于代谢靶点研究。
1.文献建立了国际上首个稳定、可标准化的人终末期纤维化肺原代AT‑Ⅱ细胞3D类器官培养体系,无血清、无滋养层、可冻存、可传代。
2.该体系能长期维持AT‑Ⅱ表型与板层小体功能,显著抑制向AT‑Ⅰ或异常基底样细胞分化。
3.纤维化来源AT‑Ⅱ类器官具有更强增殖能力,并稳定呈现疾病特异性有氧糖酵解重编程(Warburg效应),糖酵解ATP占比大幅升高。
4.该模型是研究肺纤维化上皮损伤、代谢异常、药物筛选的理想人源工具,支持精准医学与生物样本库应用。
关于晶莱