

为什么同样是类器官实验,有的团队能稳定进入机制研究、药物筛选和多组学分析,而有的团队却总停留在“偶尔能长出来”?分水岭往往不在“有没有类器官”,而在“有没有可重复、可验证、可用于后续实验的类器官体系”。
随着类器官向应用端不断深入,限制其大规模进入药筛和转化研究的,是稳定性与标准化能力
真正到了应用阶段,大家很快会碰到一连串更具体的问题:能不能稳定进入药筛?能不能顺利接上毒理、免疫共培养或转化研究?不同批次之间的结果能不能保持一致?
FDA 今年发布的 NAMs draft guidance,将 technical characterization 和数据的 quality and reliability 纳入 NAMs 验证框架的重要考虑内容;
Kim 等于 2026 年 2 月在 npj Biomedical Innovations 发表的综述中直接指出,类器官领域正在从“培养”走向“制造”,其中关键挑战就是 reproducibility 和 scalability。([U.S. Food and Drug Administration][1])
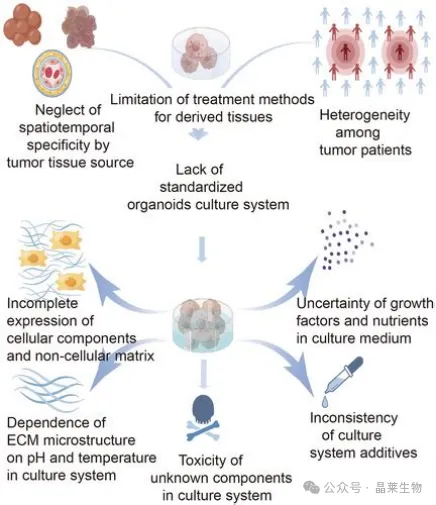
图1:标准化挑战总览图
做类器官质控,最先看的往往不是分子指标,而是形态。
边界是否完整,球体或腔体是否均一,是否存在明显塌陷、碎裂或坏死区,这些看似基础的观察,实际上直接决定了这批类器官是否值得进入下一步实验。
发布在《Nature》的一篇文章研究显示,即便在同一批次内部,类器官之间也可能存在明显异质性,因此形态学观察通常是最基础、也最有必要的前置筛查手段。
类器官“长出来”不代表“长得合适”。
如果同一批类器官在尺寸、增殖速度和成熟时间点上波动过大,后续的药筛、组学分析和功能评价都会受到批次差异的放大影响。很多时候,真正决定结果能不能比较的,并不是某一天的终点状态,而是整个生长轨迹是否一致。
尺寸和生长曲线已经越来越多地被纳入质控范围,在cerebral cortical organoids 的质量控制研究中,就把 size 和 growth profile 列为核心 QC 维度之一。
类器官能不能代表目标组织,关键不只在于有没有形成 3D 结构,更在于它的细胞组成是否符合预期。
根据不同的研究用途,这个问题的答案并不相同:
做发育研究,更关注谱系分化是否到位;
做疾病模型,更关注关键病理相关细胞有没有保留下来;
做药筛,要警惕由于细胞组成漂移带来的结果偏差。
总之,类器官“像不像目标组织”,最终还是要落到细胞组成和功能状态上。在现有 QC 框架中,cellular composition 已经被放在和形态、尺寸同样重要的位置。
进入正式实验前,还要确认这批类器官是否处在一个“健康、可解释”的状态里。
细胞毒性、DNA损伤、凋亡水平或应激状态,都会直接影响药物反应和表型输出。
类器官绝不是“长成3D结构就算活”,它必须在特定的测试窗口期内,保持可比较、可解释的状态。现有QC方法已把cell viability / cytotoxicity 纳入核心评价闭环。
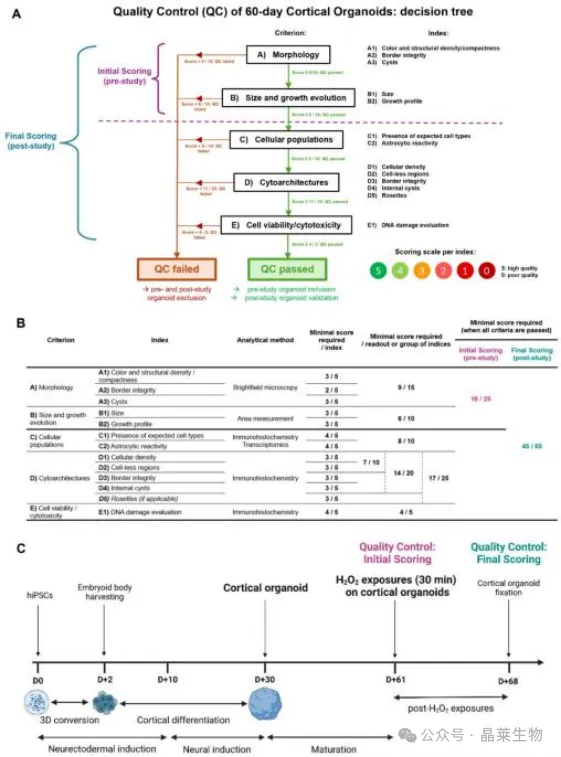
图2:QC 决策树/评分框架图
很多团队做类器官,真正拉开差距的地方,不是会不会培养,而是有没有一套清楚的“准入标准”:
1.形态学发生何种程度的畸变必须执行剔除?
2.尺寸的批内差异必须控制在什么区间?
3.生长周期的哪个阶段是药物干预的最佳窗口?
4.靶细胞组分偏离预期到什么比例需要整批废弃?
一个成熟的类器官测试平台,其核心不在于“每次都能长出来”,而是具备明确的 Go/No-Go 判定机制。
只有将不合格的批次果断拦截在测试前,后续的小分子药筛、机制研究与共培养才能拿到真正稳定的基准数据。
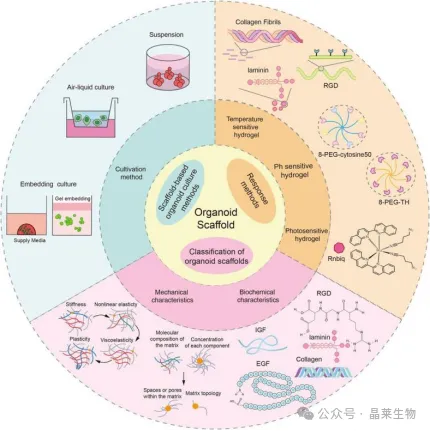
图3:scaffold / 培养微环境总览图
从目前的发展方向来看,行业不再盲目追逐“又建构了新靶点类型”,而是死磕底层技术平台的工程化
一方面,类器官芯片(organoid-on-a-chip)、3D生物打印以及自动化表征等手段,培养过程正被强制推向可控、可验证的标准化生产
对于扎根一线的科研与转化人员而言,真正的准入门槛早就变了——不是“能不能养活”,而是数据的“稳、准、可用”
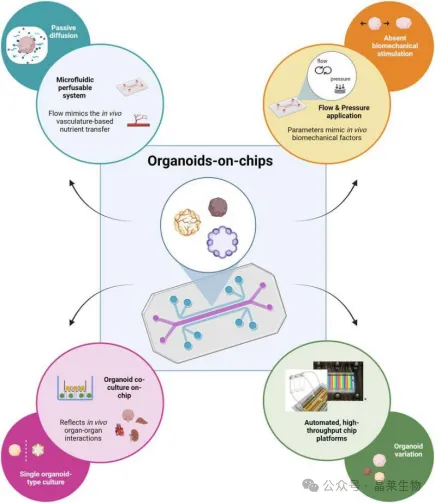
图4:organoid-on-a-chip / 工程化构建图
结语
交付数据,而不只是交付“细胞球”
上一篇,我们讨论的是肿瘤类器官为什么重要;
这一篇,我们更想补上一层——重要并不等于好用。
从“能养出来”到“能用起来”,这中间隔着一道工程化的鸿沟。对于类器官平台来说,真正的交付物永远不是几株长势良好的细胞球,而是经得起反复推敲的机制数据与药筛结果 。
关于晶莱

参考文献:
[1]: https://www.fda.gov/news-events/press-announcements/fda-releases-draft-guidance-alternatives-animal-testing-drug-development "FDA Releases Draft Guidance on Alternatives to Animal Testing in Drug Development | FDA"
[2]: https://www.nature.com/articles/s41598-025-14425-x "Towards a quality control framework for cerebral cortical organoids | Scientific Reports"
[3]: https://www.nature.com/articles/s44385-025-00054-6 "From organoid culture to manufacturing: technologies for reproducible and scalable organoid production | npj Biomedical Innovations"