
常用的癫痫模型有动物模型、脑片模型和细胞模型。
动物模型可更好地模拟癫痫发作时体内复杂的病理生理活动。
脑片模型在排除体内干扰因素(如血脑屏障、激素水平等)的同时保留了细胞在体时的微环境。
细胞模型成本相对较低、造模耗时短,在一定程度上节约资源,操作简单、结果更直观。尤其针对于药物和机制深层的分子研究,更容易排除干扰因素的细胞模型显然更为准确。
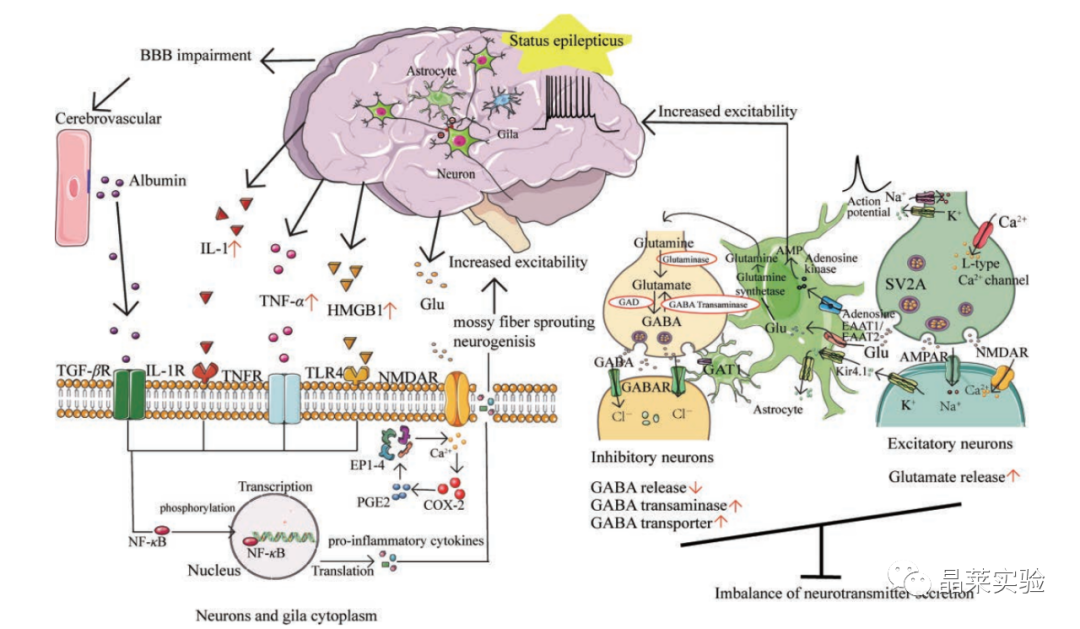
癫痫研究中主要使用的细胞模型类型有:
单细胞培养模型(如BV2小胶质细胞、原代胶质细胞、CHME3小胶质细胞、SVG星形胶质细胞等);
共培养模型(如星形胶质细胞-小胶质细胞共培养炎症模型、神经元-星形胶质细胞共培养模型等);
三培养模型(小胶质细胞-神经元-脑内皮细胞三培养模型等)。
细胞共培养根据多种细胞间是否直接接触可分为直接接触式共培养和非接触式共培养。
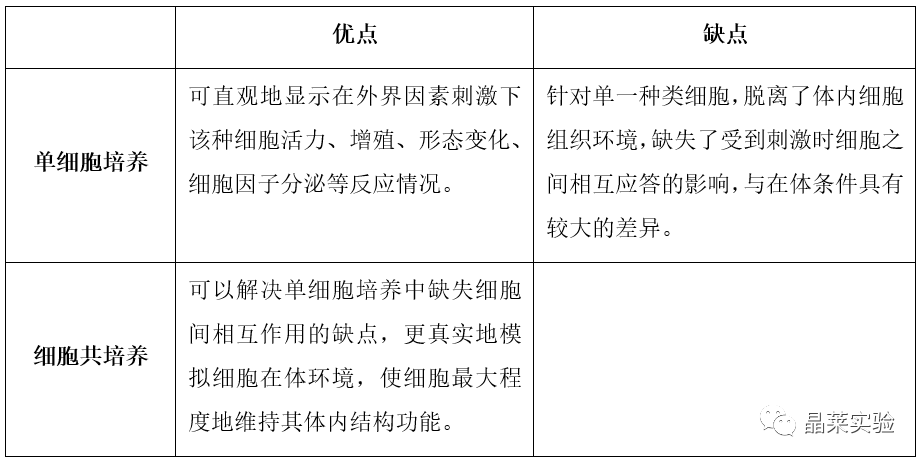
构建细胞模型所用的细胞主要分为两大类:原代细胞和商业细胞系。

1. Sombati癫痫细胞模型
Sombati癫痫细胞模型是常用的模型之一。
使用无镁或低镁细胞外液处理神经元、神经元-星形胶质细胞共培养物等细胞3小时,即可出现细胞惊厥放电,诱导自发反复性癫痫样放电的神经元模型。
原理:
Mg2+可拮抗兴奋性氨基酸,低镁细胞外液抵消了Mg2+的拮抗作用,导致细胞兴奋性增加,容易出现异常放电;
此外Mg2+是N-甲基[1]D-天冬氨酸(N-methyl-D-asparticacidreceptor,NMDA)受体—离子型谷氨酸受体的一种亚型—的拮抗剂,低Mg2+条件下NMDA离子通道开放时间延长,Ca2+内流增加。
2. 红藻氨酸(Kainicacid,KA)诱导
KA是兴奋性神经递质谷氨酸的类似物,作用于α-氨基-3-羟基-5-甲基-4-异恶唑丙酸受体导致Ca2+过量内流,引起细胞内Ca2+超载,引起神经元损伤,从而产生致痫作用。
除神经元外,KA还可以作用于神经胶质细胞,诱导神经胶质细胞增殖活化,生成促炎细胞因子,导致神经炎症,有利于癫痫中神经炎症机制的研究。
3. 其他方式
① 匹鲁卡品是动物颞叶癫痫模型的常用诱导药物,但也有研究用于建立癫痫的细胞模型。
② 谷氨酸诱导的癫痫细胞模型,用于研究卒中后癫痫的相关机制。
③ 青霉素作为最常见的抗生素之一,可能通过与抑制性神经递质γ-氨基丁酸(γ-aminobutyricacid,GABA)结合从而抑制其合成与转运而导致大脑兴奋性增高,因此可被用于实验中构建癫痫发作模型。
1. 抗癫痫发作药物 临床前对于抗癫痫发作药物的筛选及对其作用机制、靶点的研究依赖于癫痫模型。 研雷帕霉素和依维莫司 研究表明:使用脂多糖(Lipopolysaccharide,LPS)和KA处理BV2小胶质细胞建立神经炎症和癫痫细胞模型,对雷帕霉素和依维莫司两种药物在神经炎症和癫痫中的作用进行了比较,证明了依维莫司可减轻神经炎症,具有抗癫痫活性。 加巴喷丁、丙戊酸和托吡酯 研究表明在C6神经胶质瘤细胞系作为模型,研究药物在肿瘤相关癫痫中的疗效,加巴喷丁、丙戊酸和托吡酯可能是治疗肿瘤相关癫痫的有效药物。 左乙拉西坦 左乙拉西坦(Levetiracetam,LEV)是一种成熟的抗癫痫发作药物, 通过白细胞介素-1β(Interleukin-1β,IL-1β)处理星形胶质细胞-小胶质细胞共培养模型来引发炎症反应,证明了LEV通过转化生长因子-β1(Transforminggrowthfactorβ1,TGF-β1)发挥其抗炎作用,左乙拉西坦抑制了小胶质细胞和海马星形胶质细胞活化所导致的促炎因子的上调。 2. 癫痫病理生理学研究 在红藻氨酸诱导的癫痫细胞模型中,出现神经胶质细胞的活化,导致肿瘤坏死因子-α(Tumornecrosisfactor-α,TNF-α)、IL-1β、IL-12、IL-18等炎症细胞因子水平升高,证明癫痫发作导致神经炎症发生。 在LPS诱导的细胞炎症模型中,许多证据表明通过靶向Toll样受体(Toll-likereceptors,TLR)、髓样分化因子(Myeloiddifferentiationfactor88,MyD88)、核因子κB(nuclearfactorkappa-B,NF[1]κB)、丝裂原活化蛋白激酶(Mitogen-activatedproteinkinase,MAPK)、蛋白激酶B/信号传导及转录激活蛋白(ProteinkinaseB/signaltransducerandactivatoroftranscription,AKT/STAT)等信号通路,可抑制神经胶质细胞炎症发生,可能成为癫痫治疗的靶点。 星形胶质细胞表面表达缝隙连接蛋白43(Connexin43protein,Cx43),抗癫痫发作药物拉莫三嗪和托吡酯在小胶质细胞-星形胶质细胞炎症模型中诱导了Cx43表达增加,同时减少了小胶质细胞的活化,抑制了炎症反应。 Cx43可能是拉莫三嗪和托吡酯抗癫痫作用的靶点之一。 血脑屏障(Bloodbrainbarrier,BBB)可以阻止某些物质进入脑组织,是维持大脑正常生理环境的重要结构,因此与脑部疾病联系紧密。据报道,癫痫可以加重BBB的损伤,BBB损伤又会促进癫痫的发展,其可能原因是BBB渗漏的促痫成分、水通道蛋白表达改变、GABA能神经元抑制减少。 利用Transwell小室或微流控芯片可以构建BBB的细胞模型,结合癫痫细胞模型的构建方法,理论上可以构建癫痫状态下的BBB体外模型,可能会成为研究癫痫中BBB分子机制的重要工具。 3. 癫痫生物标志物 癫痫的主要生物标志物有基因生物标志物、miRNA、炎性反应性生物标志物等。目前,大多数癫痫标志物的研究集中在miRNA。 高迁移率族蛋白B1(highmobilitygroupproteinB1,HMGB1)是一种高度保守的核蛋白,在哺乳动物中广泛表达,可通过Toll样受体促进炎症反应并在癫痫中发挥重要作用。 HMGB1:使用癫痫患者手术切除的皮质和海马组织,进行显微手术解剖后进行细胞培养,分别构建3D和2D细胞模型,表明HMGB1作为炎症信号,其抗神经元性抑制了模型中海马神经元的发生。此外,已有文献报道HMGB1在区分耐药患者时表现出高特异性和选择性,可作为预测生物标志物。 如今细胞模型不断发展,在二维细胞模型的基础上已经有三维共培养模型,如组织型共培养和器官型共培养,更大程度上还原在体环境,同时又保留了细胞模型的优势。尽管如此,细胞模型仍存在不能完美复刻人体内复杂生理环境的缺点,因此可与动物模型联合使用。