
Enhanced differentiation of human pluripotent stem cells into pancreatic progenitors co-expressing PDX1 and NKX6.1
增强人多能干细胞分化为共表达PDX1和NKX6.1的胰腺祖细胞

期刊:Stem Cell Research & Therapy
发表时间:2018年
影响因子:8.088
研究背景
糖尿病作为一种以高血糖为特征的代谢性疾病,症状主要表现为“三多一少”,即多饮、多食、多尿、体重减轻,长期存在的高血糖能够导致各种组织,特别是眼、肾、心脏、血管、神经的慢性损害,严重影响了患者的生活质量和健康。
目前由于人们许多不良的饮食和生活习惯,糖尿病患者呈现出“低龄化”趋势,根据世界卫生组织(WHO)全球糖尿病报告显示,2021年糖尿病患者数量已达到5.366亿,预计2045年将增加到7.832亿,这意味着超过10.5%的世界人口患有糖尿病。
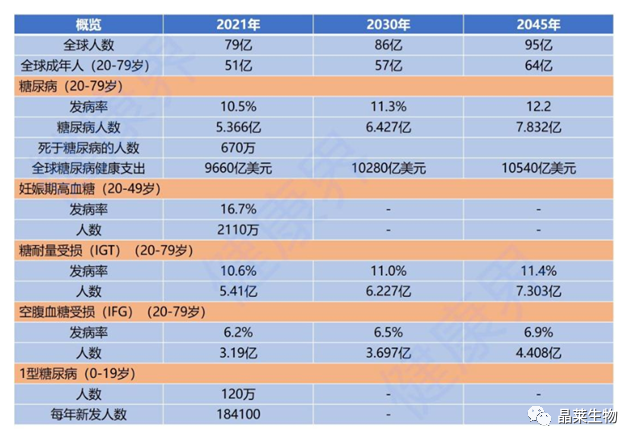
目前还没有能够治愈糖尿病的治疗手段,国内治疗手段主要是控制血糖水平尽可能接近正常,来推迟或防止进一步糖尿病并发症的发生。常规的治疗方案一般为口服降糖药以及注射胰岛素,此外体育锻炼和健康饮食对于疾病控制也发挥着关键作用。
尽管现代的胰岛素和药物疗法在不断完善,但外源性应用胰岛素永远无法像内源性β细胞分泌胰岛素一样具有准确性和动态性。长期注射胰岛素还会导致低血糖、胰岛素抵抗、体重增加等问题。
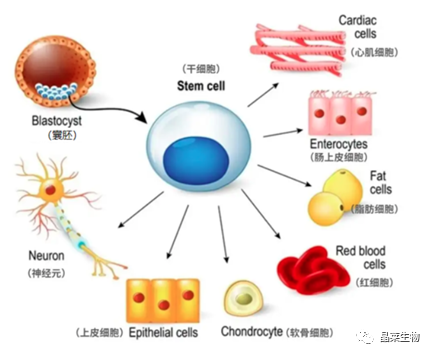
干细胞是一种具有自我更新和多向分化潜能的细胞,在一定条件下,可以分化成多种功能细胞,同时具有再生各种组织和人体器官的潜在功能。
通过技术手段来操控干细胞分化的命运,使其向着我们所需要的方向分化,可以为疑难性疾病提供新的治疗策略。
胰腺祖细胞(PP)共表达两种转录因子(TF)PDX 1和NKX6.1,被认为是功能性胰腺β细胞不可或缺的前体细胞。本文目的是建立一种有效的方案,用于最大限度地从人多能干细胞(hPSC)产生PDX 1 +/NKX6.1+ PP。
研究结果及分析
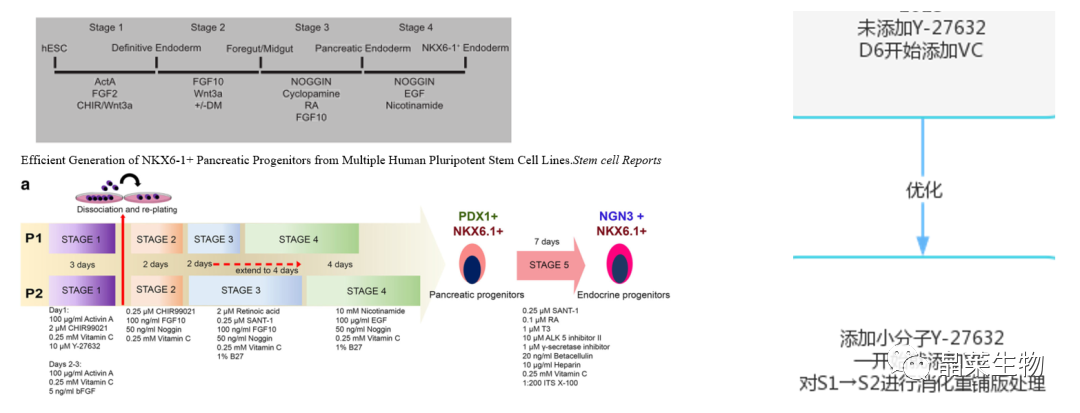
hPSC通过两种不同的方案产生胰腺祖细胞,这两种方案的第3阶段处理的持续时间不同。
hPSC-定型内胚层-前肠/中肠-胰腺内胚层-胰腺祖细胞-内分泌祖细胞。
本文优化的两种方案是来自于第一张图,优化后的方案添加了各种激活剂,通路抑制剂,以及转录因子等。P2方案在第三阶段延长了4天。
并且对两种方案又进行了消化为单细胞以内胚层细胞一半的数量重铺板处理在这里称为p1d和p2d 没有经过重新铺板的称为p1nd 和p2nd。
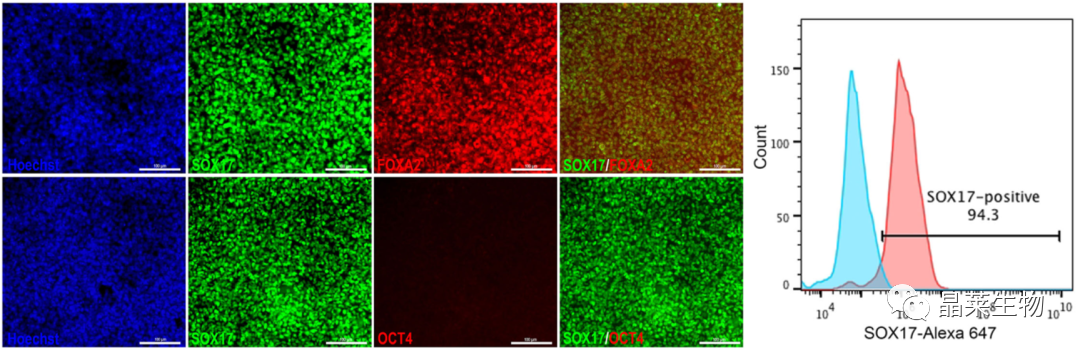
胰腺谱系细胞起源于定型内胚层,首先对发育到定型内胚层的关键基因进行检测。
免疫染色分析显示产生了表达特异性转录因子S017和F0XA2内胚层细胞。通过流式分析产生了SOX 17阳性率高达94%内胚层细胞,其进一步指向PDX 1 +/NKX6.1+祖细胞。
通过检测多能性标志物0CT4他的表达情况可以可忽略或不表达,说明目前产生的细胞丧失了它们的多能性,开始定向分化。
2. 优化分化方案以生成PDX1 / NKX6.1胰腺祖细胞++
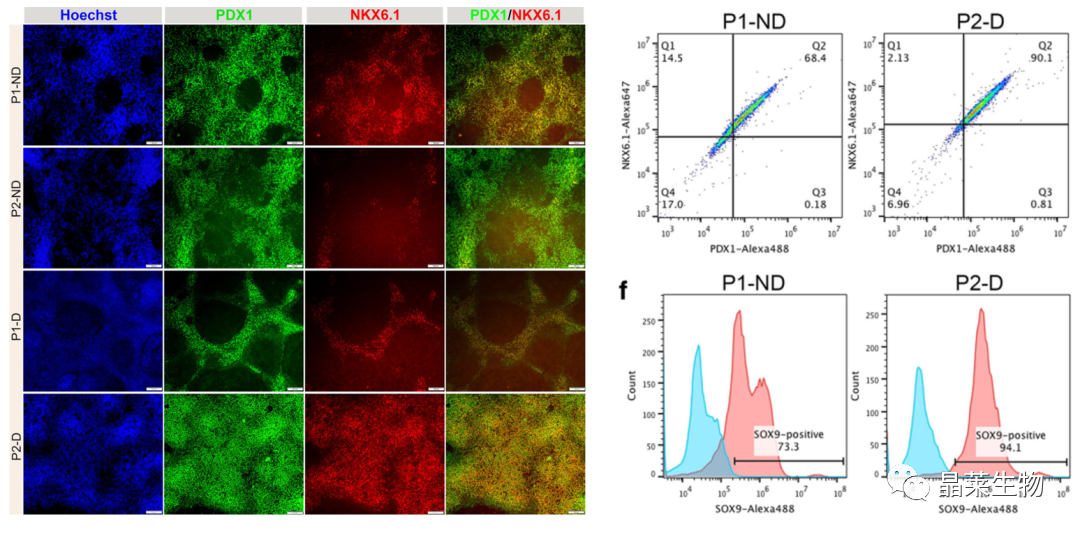
使用不同方案生成PDX1 / NKX6.1胰腺祖细胞。PDX1(绿色)和NKX6.1(红色)在由方案1非解离(P1-ND);
分化到胰腺祖细胞,通过免疫染色结果可以看到P1ND和P2D方案产生的表达两种关键转录因子的阳性细胞最高多,通过流式分析也可以证明这一点。
3. 使用不同方案生成的胰腺祖细胞中胰腺相关转录因子的mRNA表达。
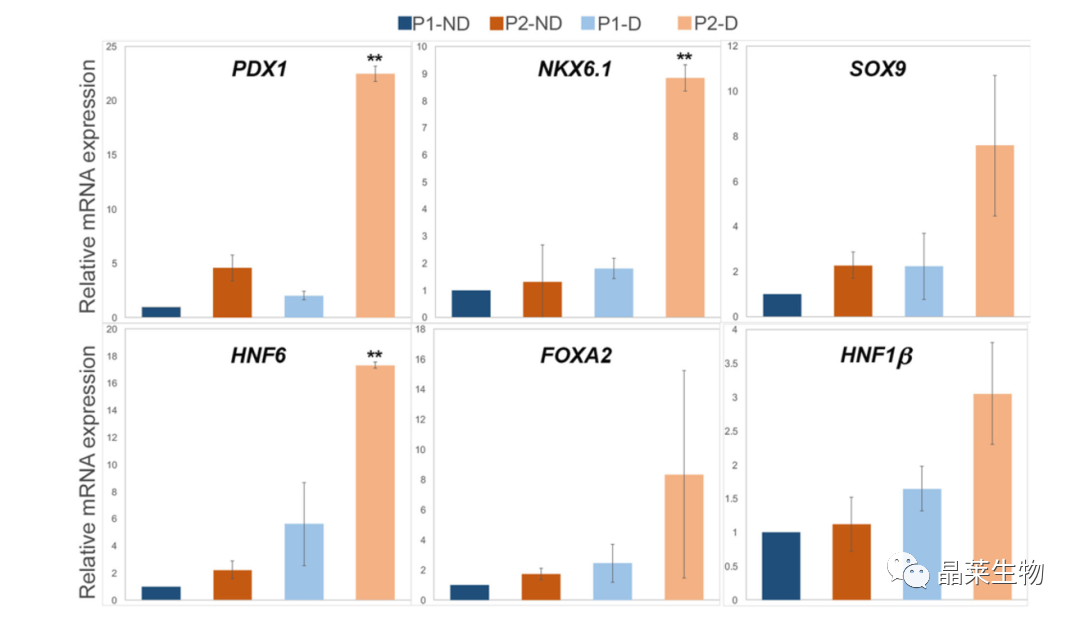
通过不同方案的第4阶段结束时胰腺TF的mRNA水平进行分析。结果显示,与所有其他方案相比,使用P2-D方案分化的胰腺祖细胞中PDX 1和NKX6.1这两种关键转录因子显著上调;
在对其他的一些胰腺发育的关键基因进行检测,也出现相同的结果。
这些结果表明,内胚层形成后消化为单细胞铺板,随后用阶段3细胞因子(P2-D)进行更长时间的诱导,增强了PDX 1 +/NKX6.1+胰腺祖细胞的产生。
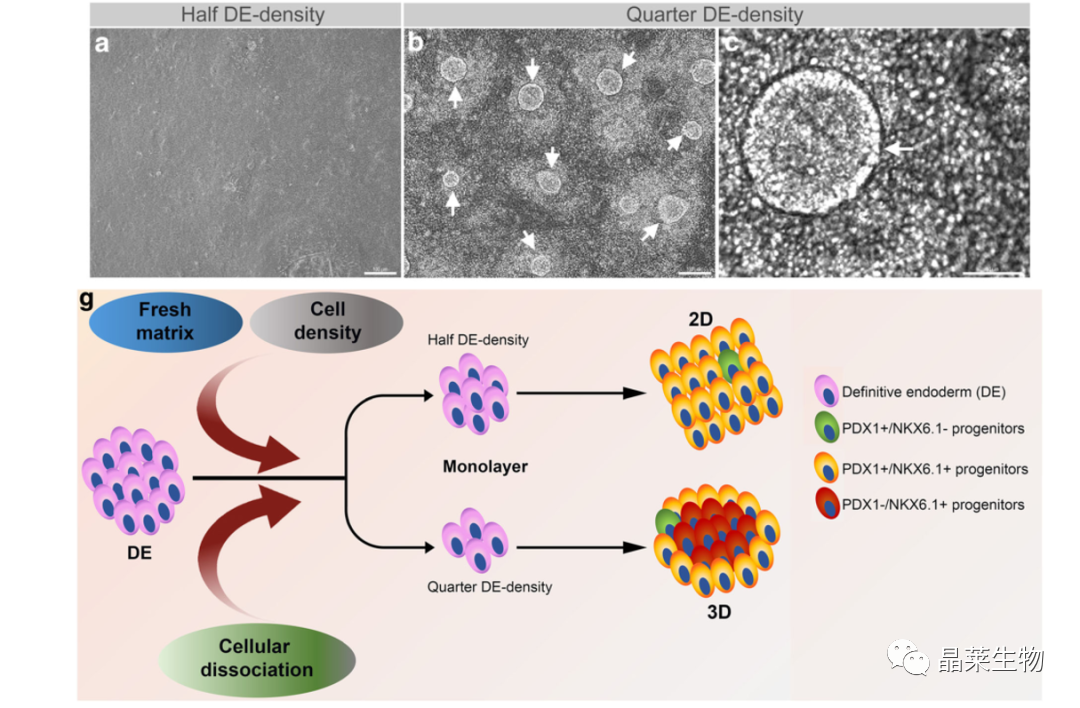
在实验过程中又产生了一种新的细胞,以约四分之一的内胚层密度(1.0-1.5 × 105个细胞/cm 2)消化并重新铺板细胞,导致了一种3D结构的出现,电镜图中看到被单层细胞包围。
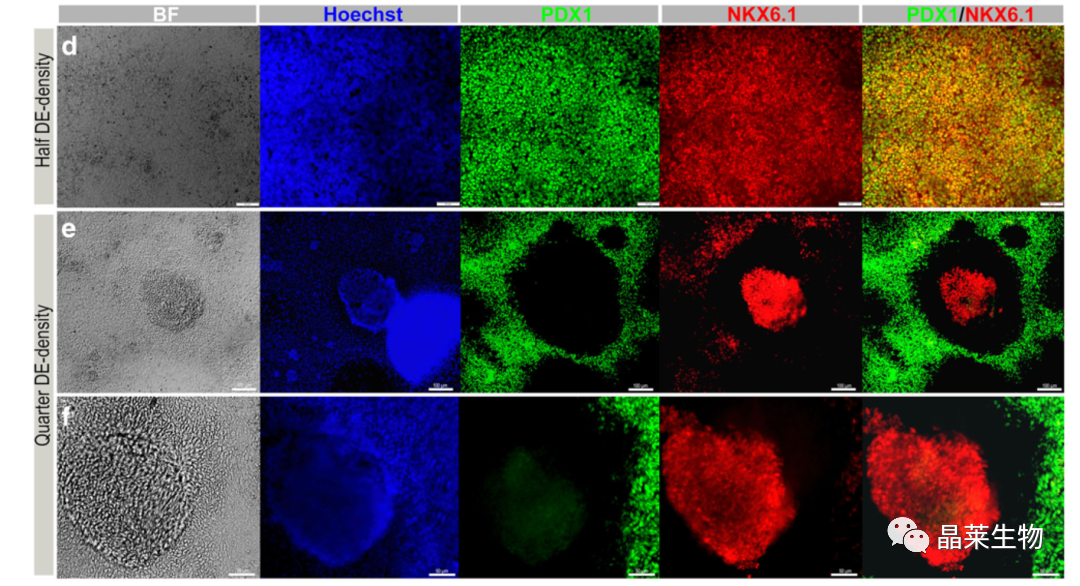
一般的密度和四分之一密度重新铺板的细胞的免疫染色分析显示,大多数单层细胞对PDXl和NKX6.1是共阳性的,而在四分之一密度培养物中出现的大多数3D结构仅对NKX6.1呈阳性(PDX 1-/NKX6.1+)。
作者推测两种胰腺祖细胞群的产生是内胚层细胞分离、细胞密度和细胞外基质对胰腺分化共同作用的结果,作者在其他文章研究了这个新细胞群体,PDX1- /NKX6.1+细胞激活了一些其他的胰腺关键基因对于分化也起到了一定作用。
5. 优化的胰腺分化方案可增加细胞增殖
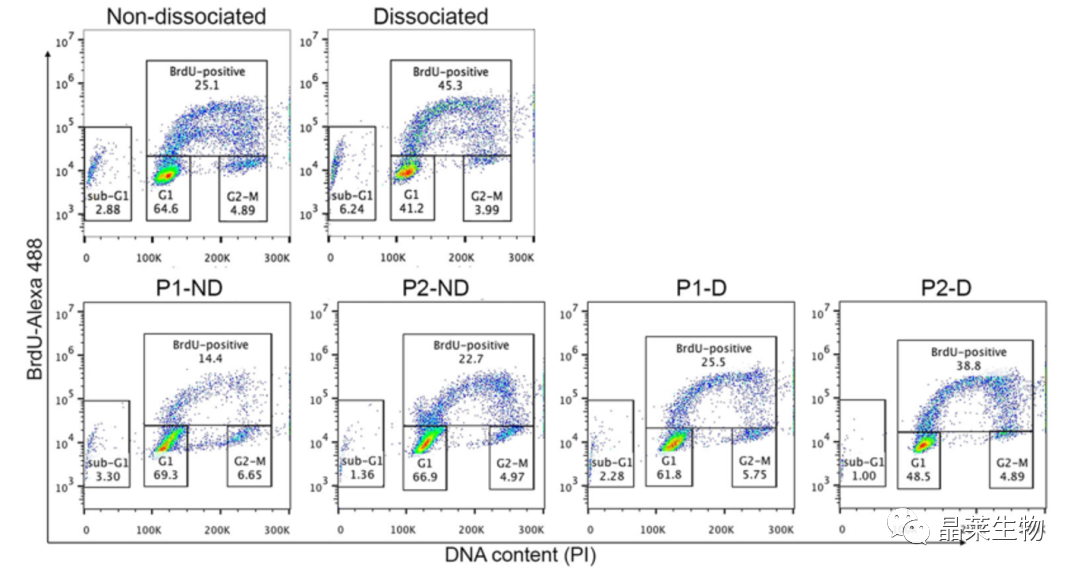
胰腺祖细胞分化的增强与细胞增殖的增加有关。
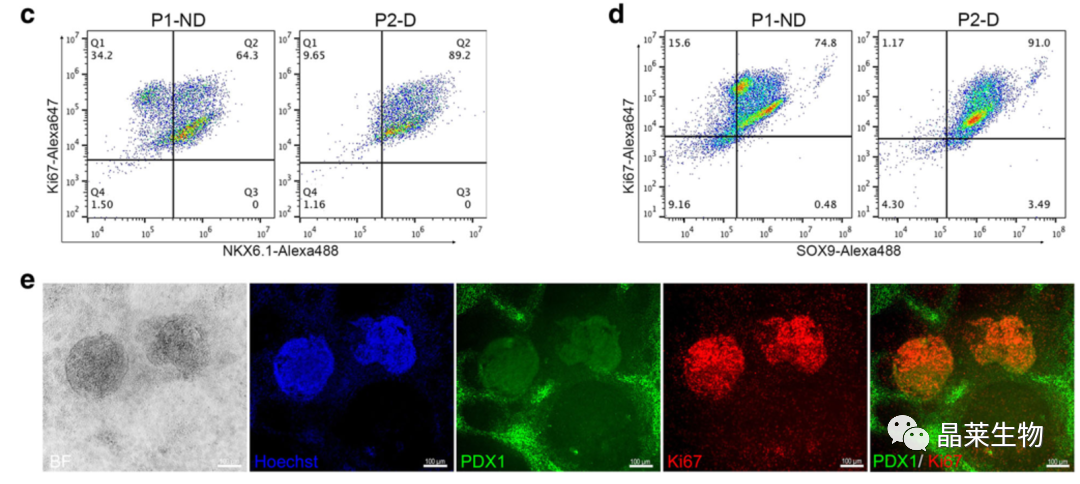
这些发现表明,优化的方案会产生高度增殖的多能胰腺祖细胞(PDX5 / NKX1.6和PDX1++++–/NKX6.1)。
6. 胰腺祖细胞分化的增强与早期肝标志物的抑制有关
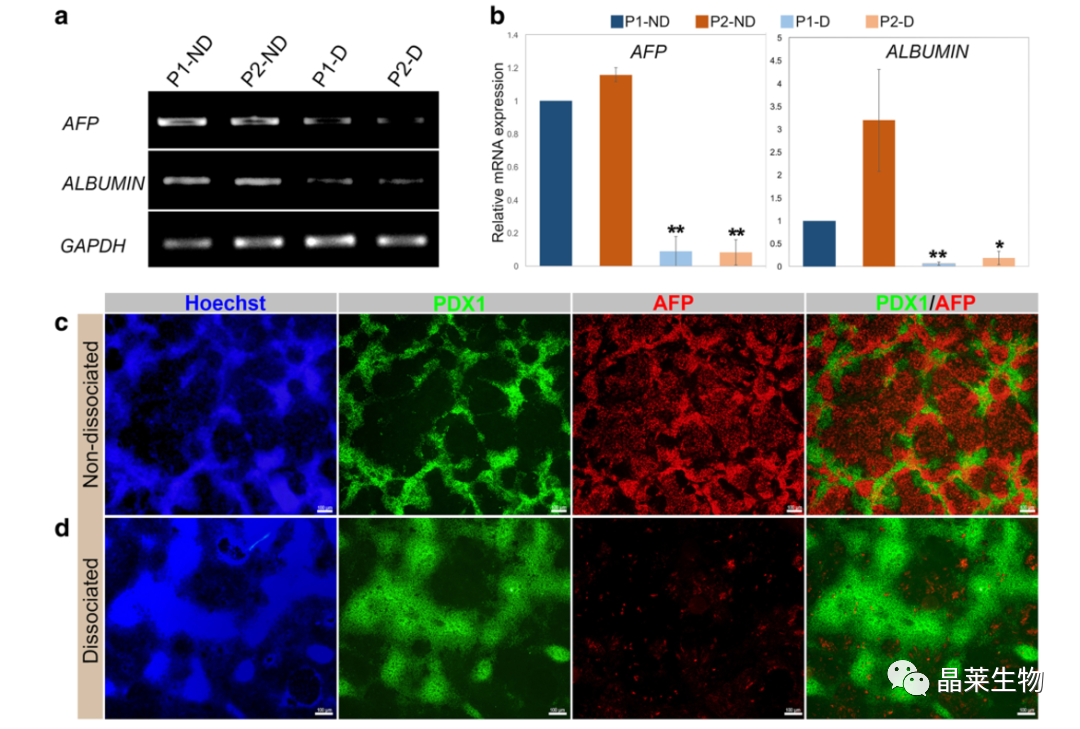
因为肝脏胰腺都是从DE发育,为了进一步确认分化效率的影响,测定了四种方案中肝脏标志性转录因子的表达水平。
结果说明,内胚层的分离通过下调早期肝脏基因AFP和ALBUMIN的表达,显著抑制了肝脏细胞谱系,从而提高了胰腺分化的效率。
7. 解离的PDX1/NKX6.1祖细胞产生内分泌祖细胞++
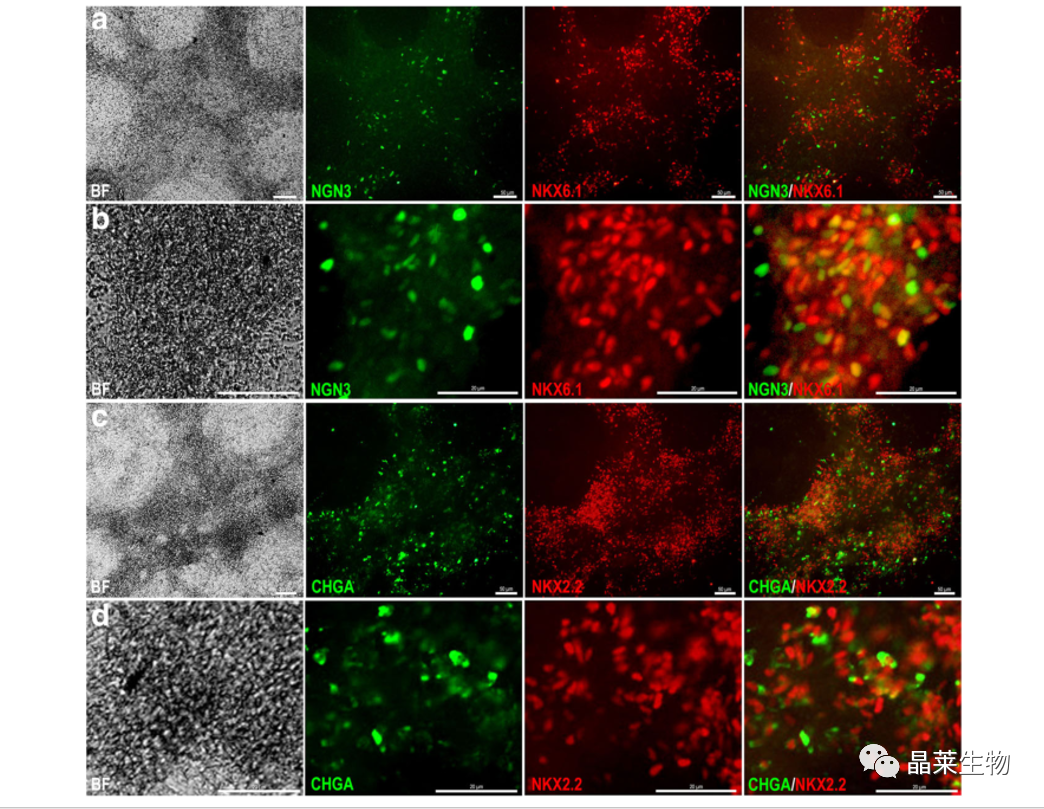
免疫染色结果显示,在第5期结束时,作者发现NGN3与NKX6.1共定位, NKX2.2与CHGA共定位。
优化方案生成的PDX1+/NKX6.1+细胞能够生成NGN3+/NKX6.1+内分泌祖细胞。诱导NGN3表达对于胰腺祖细胞调控内分泌至关重要。
这证实了P2-D方案生成的PDX1+/NKX6.1+胰腺祖细胞可以在体外粘附条件下有效地生成内分泌前体。
NKX6.1与NGN3这两个转录因子在同一内分泌前体细胞中的共定位可特异性地引导细胞向胰腺β谱系发展。产生的内分泌前体也表达了高水平的CHGA和NKX2.2,证实了它们分化为β细胞的潜力。
文献结论
本文提供了一种新的技术,产生了具有高度自我复制能力的高比例的PDXl +/NKX6.1+ PP,从而有助于在体外从hPSC可规模化地分化为功能性β细胞,也为细胞移植治疗方法提供了一种参考。
本文创新方法还产生了新的NKX6.1+/PDX 1-群体,具有内分泌前体的特征,进一步研究破译了β细胞发育的途径。
文献涉及的实验技术
关注公众号,了解更多!
